
科目: 来源:不详 题型:实验题

查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.Cu可以溶解在稀硝酸中并生成H2 |
| B.浓HNO3不能与非金属单质反应 |
| C.硝酸与金属反应时,主要是+5价的氮元素得电子 |
| D.常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.氨气极易溶于水,可以用来做喷泉实验 |
| B.氨气的还原性可以解释氨气与氯化氢的反应实验 |
| C.NH3·H2O不稳定,实验室可用NH4Cl和石灰水制取氨气 |
| D.NH3液化时放出大量的热,因而,不能用氨作制冷剂 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
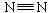 键能为945 kJ/mol,N—H键能为391 kJ/mol。写出工业合成氨反应的化学方程式 ;由键能计算说明此反应是 反应(填“吸热”或“放热”),合成氨反应(消耗1molN2 时)的△H = 。
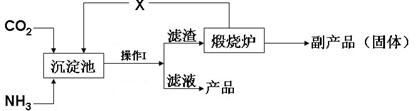
键能为945 kJ/mol,N—H键能为391 kJ/mol。写出工业合成氨反应的化学方程式 ;由键能计算说明此反应是 反应(填“吸热”或“放热”),合成氨反应(消耗1molN2 时)的△H = 。| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/(mol/L) | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目: 来源:不详 题型:填空题

查看答案和解析>>
科目: 来源:不详 题型:实验题
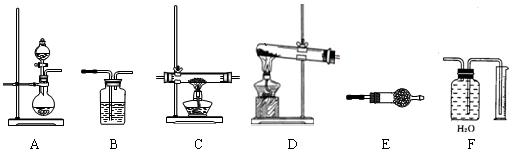
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:填空题
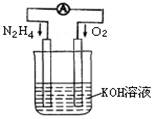
查看答案和解析>>
科目: 来源:不详 题型:填空题
| A.Na2O2 +2HCl= 2NaCl+H2O2 | B.Ag2O+ H2O2=2Ag+O2+ H2O |
| C.2 H2O2="2" H2O+O2 | D.3 H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8 H2O |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.NH3·H2O为1mol ,溶质质量为35g |
| B.NH4+为1mol ,溶质质量为18g |
| C.溶解状态的NH3分子为1mol,溶质质量为17g |
| D.氨水中NH3、NH3·H2O、NH4+三种微粒总的物质的量为1mol 。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com