
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.两种元素组成的分子中所含化学键一定是极性键 |
| B.金属晶体的熔点一定比分子晶体的高 |
| C.某晶体中含有阳离子,则一定也含有阴离子 |
| D.含有阴离子的化合物一定含有阳离子 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.分子晶体中范德华力没有方向性和饱和性,所以分子晶体一般都采取密堆积,但要受到分子形状的影响。 |
| B.由于共价键的方向性和饱和性,原子晶体堆积的紧密程度大大降低。 |
| C.配位数就是配位键的数目 |
| D.离子晶体一般都是非等径球的密堆积 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.CH4和NH是等电子体,键角均为60° |
| B.NO和CO是等电子体,均为平面正三角形结构 |
| C.H3O+和PCl3是等电子体,均为三角锥形结构 |
| D.B3N3H6和苯是等电子体,B3N3H6分子中不存在“肩并肩”式重叠的轨道 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.不是所有的共价键(σ 键)都具有方向性 |
| B.N≡N键能大于C≡C的键能,所以N≡N不易发生加成反应 |
| C.根据价层电子对互斥理论可知,OF2分子的极性小于H2O分子的极性 |
| D.Na原子基态核外电子占有3个能层,4种能级,6个原子轨道。有6种电子运动状态 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.若n=2,则分子的立体结构为V形 |
| B.若n=3,则分子的立体结构为三角锥形 |
| C.若n=4,则分子的立体结构为正四面体形 |
| D.以上说法都不正确 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 O2[PtF6],O2[PtF6]为配位化合物(其中Pt为+5价),对于此反应,下列说法正确的是
O2[PtF6],O2[PtF6]为配位化合物(其中Pt为+5价),对于此反应,下列说法正确的是| A.O2[PtF6]的配位原子是F和O,配位数为8 |
| B.此反应O2是氧化剂,PtF6是还原剂 |
| C.O2[PtF6]中Pt与F之间以离子键相结合 |
| D.每生成1mol O2[PtF6],转移1 mol电子 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
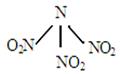
| A.分子中N、O原子间形成的共价键是非极性键 |
| B.分子中四个氮原子共平面 |
| C.该物质既有氧化性又有还原性 |
| D.分子中四个氮原子围成一个空间正四面体 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:填空题
| n+m | 2 | |
| VSEPR理想模型 | | 正四面体 |
| 价层电子对之间的理想键角 | | 109°28′ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com