
科目: 来源:不详 题型:单选题
| A.在CaF2晶体中,Ca2+、F—的配位数均为8 |
| B.C60晶体中,微粒之间通过共价键结合形成晶体,键角为120° |
| C.在CsCl晶体中,每个Cs+周围紧邻6个C1— |
| D.金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 |
查看答案和解析>>
科目: 来源:不详 题型:单选题

| A.铝的化合物的晶体中有的是离子晶体 |
| B.表中只有BCl3和干冰是分子晶体 |
| C.同族元素的氧化物可形成不同类型的晶体 |
| D.不同族元素的氧化物可形成相同类型的晶体 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.碘的升华和干冰气化 | B.二氧化硅和干冰熔化 |
| C.苯和硝酸钾熔化 | D.食盐的熔化和冰的融化 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.当中心原子的配位数为6时,配合单元常呈八面体空间结构 |
| B.SO3为平面正三角形结构 |
| C.已知[Cu(NH3)2]2+的中心原子采用sp杂化,则它们的空间构型为直线型 |
| D.配位数为4的配合物均为正四面体结构 |
查看答案和解析>>
科目: 来源:不详 题型:单选题

| A.Mg2CNi3 | B.MgCNi3 | C.MgCNi2 | D.MgC2Ni |
查看答案和解析>>
科目: 来源:不详 题型:填空题
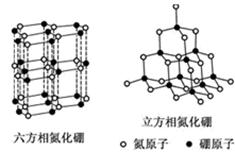
| A.立方相氮化硼含有σ键和π键,所以硬度大 |
| B.六方相氮化硼层间作用力小,所以质地软 |
| C.两种晶体中B-N键均为共价键 |
| D.两种晶体均为分子晶体 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| 物质 | NaCl | MgCl2 | AlCl3 | SiCl4 |
| 沸点/℃ | 1465 | 1412 | 181(升华) | 57.6 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
| ① | | | | | | | | | | | | | | | | | |
| | ② | | | | | | | | | | | | ③ | ④ | ⑤ | ⑥ | |
| | ⑦ | | | | | | | | | | | | | | | ⑧ | |
| | | | | | ⑨ | | | | | ⑩ | | | | | | | |
查看答案和解析>>
科目: 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com