
科目: 来源:不详 题型:单选题
| Na2O | Na | AlF3 | AlCl3 | Al2O3 | BCl3 | CO2 | SiO2 | ||||||||||||||||||||||||||
| 920℃ | 97.8℃ | 1291℃ | 190℃ | 2073℃ | -107℃ | -57℃ | 1723℃
查看答案和解析>> 科目: 来源:不详 题型:单选题 下列对物质性质的描述中属于分子晶体的是
查看答案和解析>> 科目: 来源:不详 题型:填空题 X、Y、Z、Q、W为按原予序数由小到大排列的五种短周期元素。已知:①X与Q处于同一主族,其原子价电子排布式都为n  s2np2,且X原子半径小于Q;②Y元素是地壳中含量最多的元素;W元素的电负性路小于Y元素,在W原子的价电子排布式中,p轨道上只有1个未成对电子;③Z元素的电离能数据见下表(kJ·mol-1) s2np2,且X原子半径小于Q;②Y元素是地壳中含量最多的元素;W元素的电负性路小于Y元素,在W原子的价电子排布式中,p轨道上只有1个未成对电子;③Z元素的电离能数据见下表(kJ·mol-1)
(1)XY2分子的空间构型为 。 (2)QX的晶体结构与金刚石的相似,微粒间存在的作用力是 。 (3)晶体ZW的熔点比晶体XW4明显高的原因是 。 (4)XY2在高温高压下所形成的晶胞如图所示。该晶体的类型属于 (选填“分子”、“原子”、“离子”或“金属”)漏体,该晶体中X原子的杂化形式为___ 。 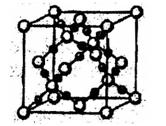 (5)氧化物MO的电子总数与QX的相等,则M为 。(填元素符号);MO是优良的耐高温材料,其晶体结构与ZW晶体结构相似,MO的熔点比CaO的高,其原因是 。 查看答案和解析>> 科目: 来源:不详 题型:单选题 某离子晶体中晶体结构最小的重复单元如图:A为阴离子,在正方体内,B为阳离子,分别在顶点和面心,则该晶体的化学式为 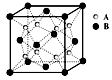
查看答案和解析>> 科目: 来源:不详 题型:填空题 (8分)选择下列物质填空(填写序号) ①氯化钙 ②干冰 ③过氧化钠 ④氯化铵 ⑤铜晶体 ⑥氩晶体 ⑦晶体硅 ⑧石墨 (1)固态时能导电的原子晶体有 (2)熔化时不破坏化学键的化合物有 (3)含有非极性共价键的离子晶体有 (4)晶体内同时存在共价键、范德华力和金属键的是 查看答案和解析>> 科目: 来源:不详 题型:填空题 (10分)计算题: 已知:晶体“二氧化硅”可由晶体“硅”衍生得到;下图是晶体“硅”及“二氧化硅”的晶胞示意图: 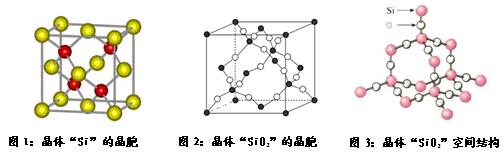 试回答: (1)请写出SiO2晶体的两种主要用途: (4分) (2)请写出与晶体SiO2化学键及晶体类型完全相同的两种物质的名称: (2分) (3)已知:二氧化硅晶体的密度为ρg/cm3 , 试求二氧化硅晶体中最近的两个Si原子之间的距离的表达式?(保留原表达式,不用化简)(4分) 查看答案和解析>> 科目: 来源:不详 题型:填空题 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F。其中A原子核外有三个未成对电子;化  合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满。请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示) 合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满。请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)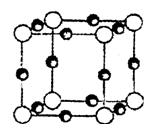 (1)A的简单氢化物分子中其中心原子采取________杂化,E的最高价氧化物分子的空间构型是____________。 (2)B的氯化物的熔点比D的氯化物的熔点________(填高或低),理由是_____________. (3)A、B、C、D的第一电离能由小到大的顺序为 _________________。(用元素符号表示) (4)A、F形成某种化合物的晶胞结构如右图所示(其中A显-3价),则其化学式为____________;(每个球均表示1个原子) (5)F的价电子轨道表示式是______________,A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,则其化学式为______________________。 查看答案和解析>> 科目: 来源:不详 题型:填空题 Ⅰ.第ⅢA、VA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型第三代半导体材料,其晶体结构与单晶硅相似。试回答: (1)Ga的基态原子的价电子的轨道排布式为 。 (2)下列说法正确的是 (选填序号)。 A.砷和镓都属于p区元素 B.GaN、GaP、GaAs均为分子晶体 C.电负性:As>Ga D.第一电离能Ga>As (3)GaAs是由(CH3)3Ga和AsH3在一定条件下制得,同时得到另一物质,该物质分子是 (填“极性分子”或“非极性分子”)。(CH3)3Ga中镓原子的杂化方式为 。 Ⅱ.氧化钙晶体的晶胞如图所示,试回答: 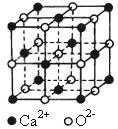 (1)晶体中Ca2+的配位数为 。 (2)已知Ca2+的半径为a cm,O2-的半径为b cm,NA代表阿伏加德罗常数, 该晶体的密度为 g/cm3。(用含a、b、NA的代数式表示) 查看答案和解析>> 科目: 来源:不详 题型:单选题 下列各组中,含有离子晶体、分子晶体、原子晶体各一种的是
查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |