
科目: 来源:不详 题型:单选题
| A.离子晶体中可能含有共价键,但不一定含有金属元素 |
| B.分子晶体中一定含有共价键 |
| C.非极性分子中一定存在非极性键 |
| D.对于组成结构相似的分子晶体,一定是相对分子质量越大,熔沸点越高 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 氧化剂或氯化剂,能与许多有机物反应。请回答下列问题:
氧化剂或氯化剂,能与许多有机物反应。请回答下列问题: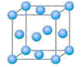
 分子的空间构型是_______。
分子的空间构型是_______。 成的合金。
成的合金。 态碳(C)原子的价电子排布式为 。
态碳(C)原子的价电子排布式为 。 )4分解为Ni和CO,从而制得高纯度的Ni粉。试推测:四羰基镍的晶体类型是 , Ni(CO)4易溶于 (填序号)。
)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测:四羰基镍的晶体类型是 , Ni(CO)4易溶于 (填序号)。 种元素的晶体竟然具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方密堆积,试写出该晶体的化学式 。晶体中
种元素的晶体竟然具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方密堆积,试写出该晶体的化学式 。晶体中 每个镁原子周围距离最近的镍原子有 个。
每个镁原子周围距离最近的镍原子有 个。
查看答案和解析>>
科目: 来源:不详 题型:填空题
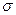 键与
键与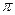 键的数目之比为
键的数目之比为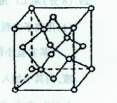
查看答案和解析>>
科目: 来源:不详 题型:填空题
 杂化,其键角比水分子 (填“大”或“小”)。
杂化,其键角比水分子 (填“大”或“小”)。
 氢键的“键能”)是 kJ / mol 。
氢键的“键能”)是 kJ / mol 。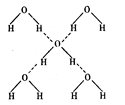
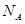 表示阿伏加德罗常数,则CaO晶胞体积为 cm3。
表示阿伏加德罗常数,则CaO晶胞体积为 cm3。查看答案和解析>>
科目: 来源:不详 题型:填空题


 )
) 按电子排布,可把周期表中的元素划分成5个区,其中j位于 区。
按电子排布,可把周期表中的元素划分成5个区,其中j位于 区。 序号“8”代表 (填元素符号);其中电负性最大的是 (填右图中的序号),第一电离能最大的是 (填图中的序号)。
序号“8”代表 (填元素符号);其中电负性最大的是 (填右图中的序号),第一电离能最大的是 (填图中的序号)。
 个π键
个π键查看答案和解析>>
科目: 来源:不详 题型:填空题
 表。
表。| 元素 | 结构或性质信息 |
| X | 原子的L层上s电子数等于p电子数。 |
| Y | 原子核外的L层有3个未成对电子。 |
| Z | 在元素周期表的各元素中电负性仅小于氟。 |
| Q | 单质常温、常压下是气体,原子的M层上有1个未成对的p电子。 |
| R | 核电荷数是Y与Q的核电荷数之和 |
| E | 原子序数比R大3 |
 共有 种不同运动状态的电子,有 种不同能级的电子。
共有 种不同运动状态的电子,有 种不同能级的电子。 物中,沸点由高到低
物中,沸点由高到低 的排列次序依次为(写化学式) 。
的排列次序依次为(写化学式) 。 l3 B.[R(H2O)5Cl]Cl2·H2O
l3 B.[R(H2O)5Cl]Cl2·H2O [R(H2O)4Cl2]Cl·2H2O D.[R(H2O)3Cl3]·3H2O
[R(H2O)4Cl2]Cl·2H2O D.[R(H2O)3Cl3]·3H2O 污染环境,其反应的化学方程式为 。
污染环境,其反应的化学方程式为 。查看答案和解析>>
科目: 来源:不详 题型:单选题
| 物质 | Na2O | NaCl | AlF3 | AlCl3 | BCl3 | Al2O3 | CO2 | SiO2 |
| 熔点 | 920 | 801 | 1291 | 190 | —107 | 2073 | —57 | 1723 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| | X | Y | Z |
| A | 混合物 | 胶体 | 分散系 |
| B | 纯净物 | 碱 | 纯碱 |
| C | 化合物 | 电解质 | BaSO4 |
| D | 化学反应 | 非氧化还原反应 | 复分解反应 |

查看答案和解析>>
科目: 来源:不详 题型:填空题
 :
: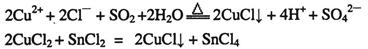
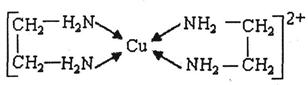
 。
。 中氮原子轨道的杂化类型为 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是_ 。
中氮原子轨道的杂化类型为 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是_ 。
查看答案和解析>>
科目: 来源:不详 题型:填空题
 构陶瓷材料的一种合成方法如下:W的氯化物与Q的氢化物加热反应,生成化合物W(QH2)4和HCL气体;W(QH2)4在高温下分解生成Q的氢化物和该陶瓷材料。上述相关反应的化学方程式(各物质用化学式表示)是 ________
构陶瓷材料的一种合成方法如下:W的氯化物与Q的氢化物加热反应,生成化合物W(QH2)4和HCL气体;W(QH2)4在高温下分解生成Q的氢化物和该陶瓷材料。上述相关反应的化学方程式(各物质用化学式表示)是 ________查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com