
科目: 来源:不详 题型:填空题
 2NH3(g) △H<0。现将10 mol N2和26 mol H2置于容积可变的密闭容器中,N2的平衡转化率(
2NH3(g) △H<0。现将10 mol N2和26 mol H2置于容积可变的密闭容器中,N2的平衡转化率( )与体系总压强(P)、温度(T)的关系如图所示。回答下列问题:
)与体系总压强(P)、温度(T)的关系如图所示。回答下列问题:
| HClO | HSCN | H2CO3 |
| K=3.210-8 | K=0.13 | Kl=4.210-7 K2=5.610-11 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 =
= mol
mol
 =
=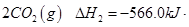 mol
mol
 =
= mol
mol

 的平衡转化率与温度、压强的关系如图a。则
的平衡转化率与温度、压强的关系如图a。则
 (填“<”、“>”或“=",下同);A、B、C三点处对应平衡常数(
(填“<”、“>”或“=",下同);A、B、C三点处对应平衡常数( )的大小关系为 ;
)的大小关系为 ;
 和2 mol
和2 mol  通入容积为1L的定容密闭容器中发生反应,能说明该反应已经达到平衡状态的是 (填序号)。
通入容积为1L的定容密闭容器中发生反应,能说明该反应已经达到平衡状态的是 (填序号)。
 的转化率为0.5,则100℃时该反应的平衡常数K= 。
的转化率为0.5,则100℃时该反应的平衡常数K= 。 、KOH(aq)设计成如图b所示的电池装置,则该电池负极的电极反应式为 。
、KOH(aq)设计成如图b所示的电池装置,则该电池负极的电极反应式为 。
查看答案和解析>>
科目: 来源:不详 题型:填空题
 CO2(g) + H2(g),反应过程中各物质的浓度如右图t1前所示变化。若保持温度不变,t2时再向容器中充入CO、H2各1mol,平衡将 移动(填“向左”、 “向右”或“不”)。t2时,若改变反应条件,导致H2浓度发生如右图t2后所示的变化,则改变的条件可能是 (填符号)。
CO2(g) + H2(g),反应过程中各物质的浓度如右图t1前所示变化。若保持温度不变,t2时再向容器中充入CO、H2各1mol,平衡将 移动(填“向左”、 “向右”或“不”)。t2时,若改变反应条件,导致H2浓度发生如右图t2后所示的变化,则改变的条件可能是 (填符号)。


查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:单选题
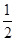 O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1| A.-417.91 kJ·mol-1 | B.-319.68 kJ·mol-1 |
| C.+546.69 kJ·mol-1 | D.-448.46 kJ·mol-1 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 2NH3的能量变化如图所示,该反应的热化学方程式是( )
2NH3的能量变化如图所示,该反应的热化学方程式是( )
A.N2(g)+3H2(g) 2NH3(l) ΔH=2(a-b-c)kJ·mol-1 2NH3(l) ΔH=2(a-b-c)kJ·mol-1 |
B.N2(g)+3H2(g) 2NH3(g) ΔH=2(b-a)kJ·mol-1 2NH3(g) ΔH=2(b-a)kJ·mol-1 |
C.N2(g)+H2(g) NH3(l) ΔH=(b+c-a)kJ·mol-1 NH3(l) ΔH=(b+c-a)kJ·mol-1 |
D.N2(g)+H2(g) NH3(g) ΔH=(a+b)kJ·mol-1 NH3(g) ΔH=(a+b)kJ·mol-1 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:单选题
 CO2(g)+2H2O(l) ΔH1=-Q1
CO2(g)+2H2O(l) ΔH1=-Q1 H2O(g) ΔH2=-Q2
H2O(g) ΔH2=-Q2 H2O(l) ΔH3=-Q3,常温下取体积比为4∶1的甲烷和氢气的混合气体11.2 L(已折合成标准状况),经完全燃烧恢复到常温,放出的热量是( )
H2O(l) ΔH3=-Q3,常温下取体积比为4∶1的甲烷和氢气的混合气体11.2 L(已折合成标准状况),经完全燃烧恢复到常温,放出的热量是( )| A.0.4Q1+0.05Q2 | B.0.4Q1+0.1Q2 |
| C.0.4Q1+0.05Q3 | D.0.4Q1+0.1Q3 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 2H2(g)+O2(g) ΔH1
2H2(g)+O2(g) ΔH1 2HCl(g) ΔH2
2HCl(g) ΔH2 4HCl(g)+O2(g) ΔH3
4HCl(g)+O2(g) ΔH3| A.ΔH3=ΔH1+2ΔH2 | B.ΔH3=ΔH1+ΔH2 |
| C.ΔH3=ΔH1-2ΔH2 | D.ΔH3=ΔH1-ΔH2 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 2CO2(g)+2H2O(l) ΔH1="-870.3" kJ·mol-1
2CO2(g)+2H2O(l) ΔH1="-870.3" kJ·mol-1 CO2(g) ΔH2="-393.5" kJ·mol-1
CO2(g) ΔH2="-393.5" kJ·mol-1 H2O(l) ΔH3="-285.8" kJ·mol-1
H2O(l) ΔH3="-285.8" kJ·mol-1 CH3COOH(l)
CH3COOH(l)| A.ΔH="+488.3" kJ·mol-1 | B.ΔH="-244.15" kJ·mol-1 |
| C.ΔH="-977.6" kJ·mol-1 | D.ΔH="-488.3" kJ·mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com