
科目: 来源:不详 题型:单选题
 C(g);△H<0,在其他条件不变时,改变其中一个条件,则生成C的速率:
C(g);△H<0,在其他条件不变时,改变其中一个条件,则生成C的速率:  CH4(g)+HC
CH4(g)+HC CH(g)+H2(g) △H1="156.6" kJ·mol-1
CH(g)+H2(g) △H1="156.6" kJ·mol-1 CH2(g)
CH2(g) CH4(g)+HC
CH4(g)+HC CH(g ) △H2="32.4" kJ·mol-1
CH(g ) △H2="32.4" kJ·mol-1 CH3CH
CH3CH CH2(g)+H2(g) 的△H= kJ·mol-1。
CH2(g)+H2(g) 的△H= kJ·mol-1。| 化学键 | C—H | C—F | H—F | F—F |
| 键能 | 414 | 489 | 565 | 158 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷高 |
| B.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷低 |
| C.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷高 |
| D.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷低 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.C + H2O ==CO + H2ΔH =+131.3kJ·mol—1 |
| B.C(s)+ H2O(g) ==CO(g) + H2(g)ΔH =+10.94kJ·mol—1 |
| C.C(s)+ H2O(g) ==CO(g) + H2(g)ΔH = -131.3kJ·mol—1 |
| D.C(s)+ H2O(g) ==CO(g) + H2(g)ΔH = +131.3kJ·mol—1 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 2NH3(g) +
2NH3(g) + 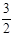 O2(g) ;△H =" a" kJ·mol—1
O2(g) ;△H =" a" kJ·mol—1| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
 2NH3(g) ΔH= -92.4kJ·mol—1
2NH3(g) ΔH= -92.4kJ·mol—1 2H2O(l) ΔH = -571.6kJ·mol—1
2H2O(l) ΔH = -571.6kJ·mol—1查看答案和解析>>
科目: 来源:不详 题型:单选题
 2SO3(g) △H=-196.64kJ/mol,当放出314.624kJ热量时,SO2的转化率为( )
2SO3(g) △H=-196.64kJ/mol,当放出314.624kJ热量时,SO2的转化率为( )| A.40% | B.50% | C.80% | D.90% |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 C(g)+D(g) ΔH =" Q" kJ/mol
C(g)+D(g) ΔH =" Q" kJ/mol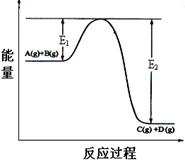
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.920 kJ | B.557 kJ | C.436 kJ | D.188 kJ |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 2SO3(g);△H=-Q kJ·mol-1(Q>0),向密闭恒容容器甲中通入l mol SO2和0.5 mol O2,向另一密闭恒容容器乙中通入2 mol SO2和1 mol O2,起始时两容器中气体的温度和压强相同,反应达到平衡时,两容器中气体的温度和压强仍相同,此时甲中放出的热量为Ql kJ,乙中放出的热量为Q2 kJ。则下列关系式正确的是 ( )
2SO3(g);△H=-Q kJ·mol-1(Q>0),向密闭恒容容器甲中通入l mol SO2和0.5 mol O2,向另一密闭恒容容器乙中通入2 mol SO2和1 mol O2,起始时两容器中气体的温度和压强相同,反应达到平衡时,两容器中气体的温度和压强仍相同,此时甲中放出的热量为Ql kJ,乙中放出的热量为Q2 kJ。则下列关系式正确的是 ( )| A.2Q1=Q2<Q | B.2Ql<Q2<Q |
| C.2Q1=Q2=Q | D.Q1<Q2=Q |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.-y kJ·mol-1 |
| B.-(10x-y)kJ·mol-1 |
| C.-(5x-0.5y)kJ·mol-1 |
| D.(10x-y)kJ·mol-1 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.② | B.③ |
| C.②③④ | D.以上都不对 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com