
科目: 来源:不详 题型:单选题
| | H2(g) | Br2(g) | HBr(g) |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | 200 | 369 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:填空题
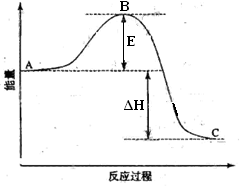
查看答案和解析>>
科目: 来源:不详 题型:填空题
 2NO(g) DH=a kJ·mol-1的平衡常数K如下表:
2NO(g) DH=a kJ·mol-1的平衡常数K如下表:| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
 2NO(g)达到平衡时N2的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
2NO(g)达到平衡时N2的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.Fe3O4 + 4CO =" 3Fe" + 4CO2△H= -14kJ·mol-1 |
| B.Fe3O4(s) + 4CO(g) =" 3Fe(s)" + 4CO2(g)△H= -22kJ·mol-1 |
| C.Fe3O4(s) + 4CO(g) =" 3Fe(s)" + 4CO2(g)△H= +14kJ·mol-1 |
| D.Fe3O4(s) + 4CO(g) =" 3Fe(s)" + 4CO2(g)△H= -14kJ·mol-1 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.已知2H2(g)+O2(g)=2H2O(l) ΔH=-483.6 kJ·mol-1,则氢气的燃烧热为483.6 kJ·mol-1 |
| B.已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
| C.已知2C(s)+2O2(g)=2CO2(g) ΔH1 2C(s)+O2(g)=2CO(g) ΔH2 则ΔH1>ΔH2 |
| D.已知Ni(CO)4(s)=Ni(s)+4CO(g) ΔH=+Q kJ·mol-1,则Ni(s)+4CO(g)=Ni(CO)4(s) ΔH=-Q kJ·mol-1 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.放热185kJ | B.吸热185kJ |
| C.放热92.5kJ | D.吸热92.5kJ |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.-44.2 kJ·mol-1 | B.+44.2 kJ·mol-1 编号 起始状态(mol) 平衡时HBr(g) 物质的量(mol) |
| C.-330 kJ·mol-1 | D.+330 kJ·mol-1 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.196.46 kJ | B.55.175 kJ |
| C.141.285 kJ | D.282.57 kJ |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.该反应中肼作还原剂 |
| B.液态肼的燃烧热为20.05 kJ·mol-1 |
| C.该动力源的突出优点之一是生成物对环境污染小 |
| D.肼和过氧化氢反应的热化学方程式为: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com