
科目: 来源:不详 题型:单选题
| A.当10 NA个电子转移时,该反应放出1300kJ的能量 |
| B.当1 NA个水分子生成且为液体时,吸收1300kJ的能量 |
| C.当2 NA个碳氧共用电子对生成时,放出1300kJ的能量 |
| D.当8 NA个碳氧共用电子对生成时,放出1300kJ的能量 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.根据热化学方程式,燃烧1mol S放出的热量为297.23 kJ |
| B.形成1 mol SO2的化学键所释放的总能量大于断裂 1 mol S ( s )和 1mol O2 ( g )的化学键所吸收的总能量 |
| C.S ( g ) + O2 ( g ) = SO2 ( g )△H =-Q kJ/mol则Q>297.23 |
| D.S ( g ) + O2 ( g ) = SO2 ( g )△H =-Q kJ/mol则Q<297.23 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.浓硫酸和NaOH溶液反应,生成 l mol水时放热57.3 kJ |
| B.含l molH2SO4的稀硫酸与足量稀NaOH溶液中和后,放热为57.3 kJ |
| C.1L 0.l mol/L CH3COOH与1L 0.l mol/L NaOH溶液反应后放热为5.73 kJ |
| D.1L 0.l mol/L HNO3与 1L 0.l mol/L NaOH溶液反应后放热为 5.73 kJ |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.1.3 | B.3.1 | C.1.6 | D.0.8 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
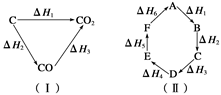
| A.ΔH1+ΔH6=ΔH2+ΔH3+ΔH4+ΔH5 |
| B.A―→D ΔH=ΔH1+ΔH2+ΔH3 |
| C.A―→F ΔH=-ΔH6 |
| D.ΔH1+ΔH2+ΔH3+ΔH4+ΔH5+ΔH6=0 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.(a+3b-2c)/2 kJ?mol-1 | B.(a+3b+2c)/6 kJ?mol-1 |
| C.(a+3b-2c)/6 kJ?mol-1 | D.(a+3b+2c)/3 kJ?mol-1 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.①②③ | B.②③ | C.①② | D.①③④ |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 O2(g)=H2O(l) △H3="-285.8KJ/mol "
O2(g)=H2O(l) △H3="-285.8KJ/mol " | A.-488.3 KJ/mol | B.+488.3KJ/mol |
| C.-245.7KJ/mol | D.+245.7KJ/mol |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 2SO3( g ) ;△ H =-QkJ·mol-1在上述条件下分别充入的气体和反应放出的热量 ( Q)如下表所列:根据以上数据,下列叙述正确的是( )
2SO3( g ) ;△ H =-QkJ·mol-1在上述条件下分别充入的气体和反应放出的热量 ( Q)如下表所列:根据以上数据,下列叙述正确的是( )| 容器 | SO2 (mol) | O2(mol) | SO3 (mol) | Q(kJ·mol-1) |
| 甲 | 2 | 1 | 0 | Q1 |
| 乙 | 1 | 0.5 | 0 | Q2 |
| 丙 | 1 | 0.5 | 1 | Q3 |

查看答案和解析>>
科目: 来源:不详 题型:填空题
 晶体释放出的热能为氯化钠晶体的晶格能。
晶体释放出的热能为氯化钠晶体的晶格能。| A.Na+(g)+Cl-(g)―→NaCl(s);△Q | B.Na(s)+Cl2(g)―→NaCl(s);△Q1 |
| C.Na(s)―→Na(g);△Q2 | D.Na(g)-e-―→Na+(g);△Q3 |
 Q5之间的关系式____
Q5之间的关系式____ 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com