
科目: 来源:不详 题型:单选题
 O2(g)= H2O(g);ΔH1=" a" kJ/mol
O2(g)= H2O(g);ΔH1=" a" kJ/mol  O2(g)=H2O(l);ΔH3=" c" kJ/mol
O2(g)=H2O(l);ΔH3=" c" kJ/mol | A.a<c<0 | B.b>d>0 | C.2c=b>0 | D.2c=d<0 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.-317.3 kJ/mol | B.-379.3 kJ/mol |
| C.-332.8 kJ/mol | D.317.3 kJ/mol |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 (1)已知:
(1)已知: H1=" 1175.7" kJ·mol-1
H1=" 1175.7" kJ·mol-1 PtF6(g) + e- = PtF6-(g)
PtF6(g) + e- = PtF6-(g)
 H2=" -" 771.1 kJ·mol-1
H2=" -" 771.1 kJ·mol-1 O2+ PtF6-(s) = O2+(g) + PtF6-
O2+ PtF6-(s) = O2+(g) + PtF6-  H3="482.2" kJ·mol-1
H3="482.2" kJ·mol-1  则反应O
则反应O 2(g)+ PtF6 (g) = O2+PtF6- (s)
2(g)+ PtF6 (g) = O2+PtF6- (s)  H="_____________" kJ·mol-1
H="_____________" kJ·mol-1 J。该反应的热化学方程式为________。
J。该反应的热化学方程式为________。查看答案和解析>>
科目: 来源:不详 题型:填空题
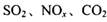 是对环境影响较大的儿种气体,对它们的合理控制和治理是优化我们生存环境的有效途径。
是对环境影响较大的儿种气体,对它们的合理控制和治理是优化我们生存环境的有效途径。 浓度的有__________ (选填字母)。
浓度的有__________ (选填字母)。


 条件下,
条件下,
 ,其平衡常数K=13.3。
,其平衡常数K=13.3。 ,则
,则 =_______________(保留两位有效数字)。
=_______________(保留两位有效数字)。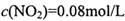 ,
, ,则改变的条件是____________________
,则改变的条件是____________________查看答案和解析>>
科目: 来源:不详 题型:填空题

查看答案和解析>>
科目: 来源:不详 题型:单选题

| A.404 | B.260 | C.230 | D.200 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 (2)2Zn(s)+O2(g)=2ZnO(s) Δ
(2)2Zn(s)+O2(g)=2ZnO(s) Δ H1 =" —702" kJ/mol
H1 =" —702" kJ/mol 2Hg(l)+O2(g)=2HgO(s) ΔH2 =" —182" kJ/mol
2Hg(l)+O2(g)=2HgO(s) ΔH2 =" —182" kJ/mol
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:单选题
 联氨(N2H4) 为燃料、过氧化氢为助燃剂。已知下列各物质反应的热化学方程式:
联氨(N2H4) 为燃料、过氧化氢为助燃剂。已知下列各物质反应的热化学方程式:| A.N2H4(g)+2H2O2(l)= N2(g)+4H2O(l)ΔH=-817.63 kJ·mol-1 |
| B.N2H4(g)+2H2O2(l)= N2(g)+4H2O(g)ΔH=-817.63 kJ·mol-1 |
| C.N2H4(g)+2H2O2(l)= N2(g)+4H2O(l)ΔH=-641.63 kJ·mol-1 |
D.N2H4(g)+2H2O2(l)= N2(g)+4H2O( g)ΔH=-641.63 kJ·mol-1 g)ΔH=-641.63 kJ·mol-1 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 O2(g)=H2O(l) ;ΔH 3=-285.8kJ/mol
O2(g)=H2O(l) ;ΔH 3=-285.8kJ/mol | A.488.3 kJ/mol | B.-488.3 kJ/mol | C.-244.15 kJ/mol | D.244.15 kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com