
科目: 来源:不详 题型:问答题
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| H2O | CO | CO2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
科目: 来源:不详 题型:问答题
 HCO3-+H+的平衡常数K1=______.(已知:10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1=______.(已知:10-5.60=2.5×10-6)查看答案和解析>>
科目: 来源:不详 题型:问答题
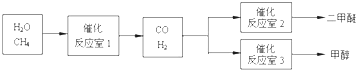
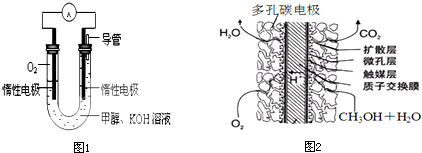
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:填空题
| ||
| ||
| ||
查看答案和解析>>
科目: 来源:不详 题型:单选题
| 3 |
| 2 |
| A.-2491kJ?mol-1 | B.+859kJ?mol-1 |
| C.-1403kJ?mol-1 | D.-859kJ?mol-1 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
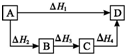
| A.△H1=△H2=△H3=△H4 | B.△H1+△H2=△H3+△H4 |
| C.△H1+△H2+△H3=△H4 | D.△H1=△H2+△H3+△H4 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
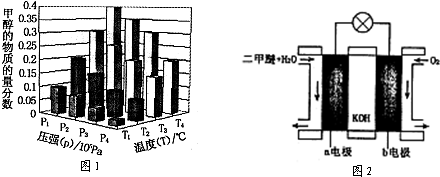
| 催化剂 |
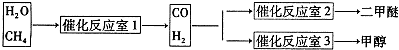
查看答案和解析>>
科目: 来源:不详 题型:填空题
| ||
| 1 |
| 2 |
| 1 |
| 2 |
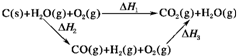
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com