
科目: 来源:不详 题型:单选题

| A.a点时,溶液呈碱性,溶液中c(B+)>c(Cl-) |
| B.b点时溶液的pH=7 |
| C.当c(Cl-)=c(B+)时,V(HCl)<20mL |
| D.C点时溶液中c(H+)约为0.03mol/L |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.c(Na+)=c(Y-)+c(HY) |
| B.c(OH-)=c(H+)+c(HY) |
| C.c(Y-)>c(Na+)>c(OH-)>c(H+) |
| D.c(Na+)+c(H+)=c(OH-)+c(Y-) |
查看答案和解析>>
科目: 来源:不详 题型:单选题
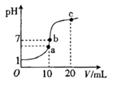
| A.在a点:c(Cl-)>c(NH4+)>c(Cl-)>c(OH-) |
| B.在b点:c(H+)=c(OH-),c(NH4+)=c(Cl-) |
| C.在b点.盐酸与氨水恰好完全中和 |
| D.在c点:c(NH4+)+c(NH3·H2O)=2c(Cl-) |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.95℃时纯水的pH<7,说明加热可导致水呈酸性 |
| B.将pH=3的CH3COOH溶液加水稀释10倍后pH=4 |
| C.0.2 mol/L的盐酸1L加水到2L后,溶液的pH=1 |
| D.NaHCO3溶液水解反应的方程式: HCO3-+ H2O = H3O++ CO32- |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.1×10-7mol·L-1 | B.1×10-12mol·L-1 |
| C.1×10-2mol·L-1 | D.1×10-14mol·L-1 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.a=b | B.a>b | C.c(A-)= c(Na+) | D.c (A-)< c(Na+) |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:计算题
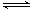 W (s) + 2H2O (g);ΔH= +66.0 kJ· mol-1
W (s) + 2H2O (g);ΔH= +66.0 kJ· mol-1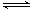 W (s) + 2H2O (g);ΔH = -137.9 kJ· mol-1
W (s) + 2H2O (g);ΔH = -137.9 kJ· mol-1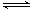 WO2 (g) 的ΔH = ______________________。
WO2 (g) 的ΔH = ______________________。查看答案和解析>>
科目: 来源:不详 题型:实验题
| 滴定次数 | 待测液体积 (mL) | 标准KMnO4溶液体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 3.00 | 23.00 |
| 第三次 | 25.00 | 4.00 | 24.10 |
| 难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com