
科目: 来源:不详 题型:单选题
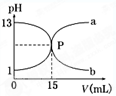
| A.盐酸的物质的量浓度为1 mol/L |
| B.P点时反应恰好完全,溶液呈中性 |
| C.曲线a是盐酸滴定氢氧化钠的滴定曲线 |
| D.酚酞不能用作本实验的指示剂 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:填空题
| A.固体CH3COOK | B.固体CH3COONH4 | C.气体NH3 | D.固体NaHCO3 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.将pH=3的醋酸稀释后,溶液中所有离子的浓度均降低 |
| B.在纯水中加入少量NaOH或醋酸钠均可抑制水的电离 |
| C.常温下,将pH=3的盐酸和pH=11的氨水等体积混合,溶液的pH>7 |
| D.用标准NaOH溶液滴定醋酸至刚好完全反应时,溶液中C(Na+)=C(CH3COO-) |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.若HA为弱酸,BOH为弱碱,则有C(H+)+C(B+)===C(OH-)+ C(A-) |
| B.若HA为强酸,BOH为弱碱,则有C(A-)>C(B+) >C(H+) >C(OH-) |
| C.若HA为弱酸,BOH为强碱,则有C(B+) >C(A-) >C(OH-) >C(H+) |
| D.若HA为强酸,BOH为强碱,则有C(H+)= C(A-)= C(B+)= C(OH-)=0.1mol·L-1 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:实验题
| A.用标准溶液润洗滴定管2~3次 |
| B.取标准KOH溶液注入碱式滴定管至刻度0以上2~3cm |
| C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液 |
| D.调节液面至0或0以下刻度,记下读数 |
| 实验次数 | c(KOH)/mol·L-1 | B中起点刻度 | B中终点刻度 | V(HCl)/ml |
| 1 | 0.1000 | 0 | 24.95 | 25.00 |
| 2 | 0.1000 | 0 | 24.96 | 25.00 |
| 3 | 0.1000 | 0 | 24.50 | 25.00 |
| 4 | 0.1000 | 0 | 24.94 | 25.00 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.2H2(g) + O2(g) ==2H2O(l)ΔH==-572kJ·mol—1 |
| B.KOH(aq)+ CH3COOH (aq) =CH3COOK (aq)+H2O(l);△H=-57.3 kJ·mol–1 |
| C.C8H18(l)+ 12.5O2 (g) = 8CO2 (g)+ 9H2O(l);△H=-5518 kJ·mol–1 |
| D.CH4(g) + 2O2(g) ==CO2(g) + 2H2O(g)ΔH==-533kJ·mol—1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com