
科目: 来源:不详 题型:单选题
| A.钢铁发生析氢腐蚀时,负极电极反应是Fe-2e-=Fe2+ |
| B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
| C.将pH=4的盐酸和醋酸稀释成pH=5的溶液,盐酸所需加入的水多 |
| D.一定温度下,反应MgCl2(l)=Mg(l)+ Cl2(g)的△H>0△S>0 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.1.7 | B.2.0 | C.12.0 | D.12.4 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.-67.7 kJ/mol | B.-43.5 kJ/mol |
| C.+43.5 kJ/mol | D.+67.7 kJ/mol |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
查看答案和解析>>
科目: 来源:不详 题型:实验题
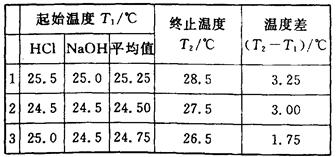
| A.溶液混合后未及时盖好量热计杯盖 |
| B.倾倒溶液太快,有少量溅出烧杯 |
| C.溶液混合后搅拌不够 |
| D.未等温度升到最高值就记录温度计示数 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.m>n | B.m=n | C.m<n | D.不能确定 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:填空题
 CH3COO- + H+
CH3COO- + H+查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.混合液的pH=7 | B.a=b |
| C.混合液中Kw=[c(H+)]2 | D.a=b,VA=VB |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com