
科目: 来源:不详 题型:单选题
| A.c(NH)相等的(NH4)2SO4溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2]<c[(NH4)2SO4]<c(NH4Cl) |
| B.0.1 mol·L-1的CH3COOH溶液加水稀释,溶液中c(OH-)减小 |
| C.0.2 mol·L-1 HCl溶液与等体积0.05 mol·L-1 Ba(OH)2溶液混合后,溶液的pH=1 |
| D.0.2 mol·L-1的NaHCO3溶液中c(H+)+c(H2CO3)=2c(CO)+c(OH-) |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.加水稀释10倍后,pH=4 |
| B.加水稀释后,溶液中c(H+)和c(OH-)均减少 |
| C.加入醋酸钠晶体后,溶液的pH增大 |
| D.加入等体积、pH=11的NaOH溶液后,c(Na+)= c(CH3COO-) |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.空气能热水器、沼气的利用、乙醇汽油都涉及到生物质能的利用 |
| B.李比希燃烧法、钠熔法、铜丝燃烧法、纸层析法都是元素定性分析法 |
| C.钢筋混凝土、玻璃钢、石棉瓦、碳纤维增强陶瓷都是常见的复合材料 |
| D.液化、汽化、风化、熔化等都是物理变化 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.H2热值为142.9 kJ·g-1,则氢气燃烧的热化学方程式可表示为: 2H2(g)+ O2(g)= 2H2O(l)△H=-285.8kJ·mol-1 |
| B.Al3+、Cu2+、SO42-、F-能在溶液中大量共存 |
| C.硫酸亚铁溶液在空气中发生氧化反应:4 Fe2++ O2+4H+= 4 Fe3++2H2O |
| D.已知KSP(Ag2SO4)= 1.4×10—5,则向100mL0.01mol·L—1的Na2SO4溶液中加入1 mL0.01mol·L—1的AgNO3溶液,有白色沉淀生成 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.100℃时,pH=12的NaOH溶液和pH=2的H2SO4恰好中和,所得溶液的pH=7 |
| B.25℃时,0.2 mol/L Ba(OH)2溶液和0.2 mol/L HCl等体积混合,所得溶液的pH=7 |
| C.25℃时,0.2 mol/LNaOH溶液与0.2 mol/L CH3COOH恰好中和,所得溶液的pH=7 |
| D.25℃时,pH=12的氨水和pH=2的H2SO4等体积混合,所得溶液的pH>7 |
查看答案和解析>>
科目: 来源:不详 题型:单选题

| A.曲线Ⅱ为醋酸稀释时的变化曲线 |
| B.a、b、c三点溶液的pH大小顺序为a>b>c |
| C.a点的Kw值比b点的Kw值大 |
| D.b点水电离的H+物质的量浓度小于c点水电离的H+物质的量浓度 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 (填序号)。
(填序号)。
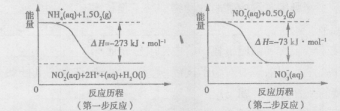
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.404 KJ/mol | B.260 KJ/mol | C.230 KJ/mol | D.200 KJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com