
科目: 来源:不详 题型:单选题
| A.Na2CO3 | B.CH3COONa | C.NaOH | D.NaHCO3 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
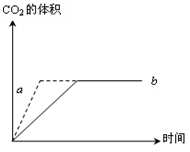
 2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。| 编号 | 改变的条件 | 生成SO3的速率 |
| ① | 升高温度 | |
| ② | 降低温度 | |
| ③ | 增大氧气的浓度 | |
| ④ | 使用催化剂 | |
| ⑤ | 压缩体积 | |
| ⑥ | 恒容下充人Ne | |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 ②如果实验过程中所用的盐酸是过量的,则所取块状石灰石与粉末状石灰石的质量是否相等?(填“相等”或“不相等”)。
②如果实验过程中所用的盐酸是过量的,则所取块状石灰石与粉末状石灰石的质量是否相等?(填“相等”或“不相等”)。查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.改用98%的浓硫酸 | B.改用铝粉 |
| C.改加入2 mol/L的稀硫酸100 mL | D.加热 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.一定条件下,增大反应物的量会加快化学反应速率 |
| B.增大压强,肯定会加快化学反应速率 |
| C.活化分子间所发生的碰撞为有效碰撞 |
| D.能够发生有效碰撞的分子叫活化分子 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 H2O2
H2O2 2H
2H → 2Fe
→ 2Fe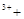 2H2O 2Fe
2H2O 2Fe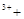 H2O2 → 2Fe
H2O2 → 2Fe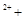 O2↑
O2↑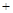 2H
2H
A.H2O2的氧化性比Fe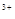 强,其还原性比Fe 强,其还原性比Fe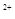 弱 弱 |
| B.在H2O2分解过程中,溶液的pH逐渐下降 |
C.在H2O2分解过程中,Fe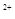 和Fe 和Fe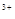 的总量保持不变 的总量保持不变 |
D.H2O2生产过程要严格避免混入Fe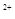 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
| 烯类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
查看答案和解析>>
科目: 来源:不详 题型:实验题

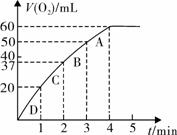
查看答案和解析>>
科目: 来源:不详 题型:填空题
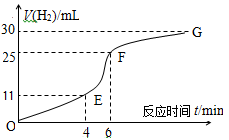
| A.蒸馏水 | B.氯化钠固体 | C.氯化钠溶液 | D.浓盐酸 E.降低温度 |
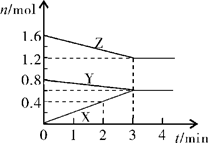
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.蒸馏水 | B.加热 | C.NaCl固体 | D.浓盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com