
科目: 来源:不详 题型:单选题
| A.将H2SO4溶液改为浓硫酸 | B.用1mol/LH2SO4溶液代替原H2SO4溶液 |
| C.用锌粉代替块状锌 | D.用同浓度热的H2SO4溶液代替原H2SO4溶液 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
A. 是可逆反应 是可逆反应 |
| B.在可逆反应中,使用催化剂可以同等程度的改变正、逆反应速率 |
| C.任何可逆反应的反应限度都相同 |
| D.在可逆反应中,使用催化剂会增大正反应速率,减小逆反应速率 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
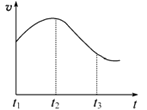
查看答案和解析>>
科目: 来源:不详 题型:填空题
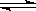 H2+I2 Ⅲ.2H2SO4===2SO2+O2+2H2O
H2+I2 Ⅲ.2H2SO4===2SO2+O2+2H2O
查看答案和解析>>
科目: 来源:不详 题型:单选题
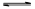 pC(g) △H 在密闭容器器中进行,如图所示,反应在不同时间t、温度T和压强P与反应混合物在混合气体中的百分含量(B%)的关系曲线,由曲线分析下列判断正确的是
pC(g) △H 在密闭容器器中进行,如图所示,反应在不同时间t、温度T和压强P与反应混合物在混合气体中的百分含量(B%)的关系曲线,由曲线分析下列判断正确的是 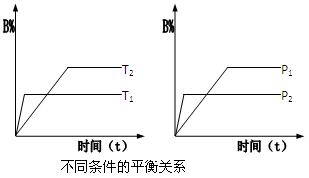
| A.T1<T2,p1>p2,m+n>p,△H>0 |
| B.T1>T2,p1<p2,m+n>p,△H>0 |
| C.T1>T2,p1<p2,m+n<p,△H<0 |
| D.T1>T2,p1>p2,m+n>p,△H<0 |
查看答案和解析>>
科目: 来源:不详 题型:实验题
| 实验过程 | 实验现象 | 结论 |
| 向盛有5 mL 5%的H2O2溶液的试管中滴入少量的 HCl,把带火星的木条伸入试管. | 无明显现象 | |
| 向盛有5 mL 5%的H2O2溶液的试管中滴入少量的Fe2(SO4)3,把带火星的木条伸入试管. | 试管中有大量气泡产生,带火星的木条复燃 | |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.使用催化剂可以增大正反应速率,减小逆反应速率 |
| B.使用催化剂可以使化学平衡向正反应方向移动 |
| C.使用催化剂可以降低反应的活化能 |
| D.使用催化剂可以改变反应的平衡常数 |
查看答案和解析>>
科目: 来源:不详 题型:实验题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标准状况) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.有些药物的标签上注明必须冷藏 |
| B.铵态氮肥与草木灰不能同时施用 |
| C.在接触室中加入五氧化二钒使二氧化硫与氧气在其表面反应 |
| D.劈碎的木材燃烧更旺 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 2 NH3 (g) ΔH<0,达平衡后,将气体混合物的温度降低,下列叙述中正确的是
2 NH3 (g) ΔH<0,达平衡后,将气体混合物的温度降低,下列叙述中正确的是| A.正反应速率增大,逆反应速率减小,平衡一定向正反应方向移动 |
| B.正反应速率减小,逆反应速率减小,平衡一定向逆反应方向移动 |
| C.若同时扩大容器的体积,则正逆反应速率一定都减小,平衡向逆反应方向移动 |
| D.若温度降低至氨气液化,则平衡一定向正反应方向移动,氨气产率提高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com