
科目: 来源:不详 题型:单选题
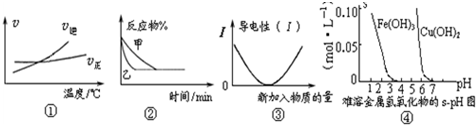
| A.根据图①可判断可逆反应A2(g)+3B2(g)?2AB3(g)正反应是吸热反应 |
| B.图②表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 |
| C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
| D.根据图④溶解度与溶液pH关系,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO,调节至pH在4左右 |
查看答案和解析>>
科目: 来源:不详 题型:问答题

查看答案和解析>>
科目: 来源:不详 题型:多选题
A. | B. | C. | D. |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| 压强\A转化率\温度 | p1(MPa) | p2(MPa) |
| 400℃ | 99.6 | 99.7 |
| 500℃ | 96.9 | 97.8 |
A.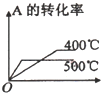 | B.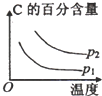 | C.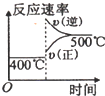 | D.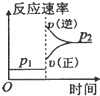 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
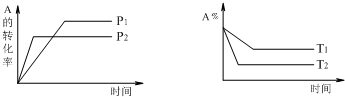
| A.a+b<c+d;正反应吸热 | B.a+b>c+d;正反应放热 |
| C.a+b<c+d;正反应放热 | D.a+b>c+d;正反应吸热 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
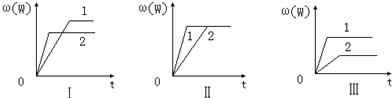
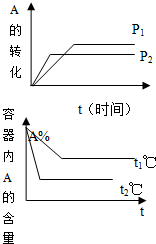
| A.图Ⅰ可能是不同压强对反应的影响,且P2>P1,a+b>n |
| B.图Ⅲ可能是不同温度对反应的影响,且T1>T2,Q<0 |
| C.图Ⅱ可能是不同压强对反应的影响,且P1>P2,n<a+b |
| D.图Ⅱ可能是在同温同压下催化剂对反应的影响,且1使用的催化剂效果好 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
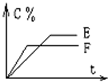
查看答案和解析>>
科目: 来源:不详 题型:问答题
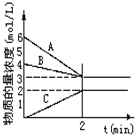
查看答案和解析>>
科目: 来源:不详 题型:问答题
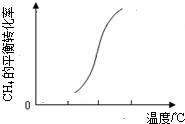 则△H2______0(填“<”、“>”或“=”).在T℃时的1L密闭容器中,充入1molCH4和3molH2O(g),发生反应②,经过5min达到平衡,此时CH4的转化率为50%,则从开始到平衡,H2的平均反应速率为______,T℃时该反应的平衡常数为______;
则△H2______0(填“<”、“>”或“=”).在T℃时的1L密闭容器中,充入1molCH4和3molH2O(g),发生反应②,经过5min达到平衡,此时CH4的转化率为50%,则从开始到平衡,H2的平均反应速率为______,T℃时该反应的平衡常数为______;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com