
科目: 来源:不详 题型:单选题

| A.氯化钠是由钠离子和氯离子构成的 |
| B.氯化钠的电离方程式为:NaCl =Na+ + Cl— |
| C.氯化钠的电离过程需要通电才能完成 |
| D.氯化钠在水中形成能自由移动的水合钠离子和水合氯离子 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.加适量的醋酸钠晶体后,两溶液的pH均增大 |
| B.温度升高20℃后,两溶液pH均不变 |
| C.加水稀释2倍后,两溶液的pH同等程度减小 |
| D.加足量的锌充分反应后,两溶液中产生的氢气一样多 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.强电解质的导电能力一定大于弱电解质的导电能力 |
| B.溶于水能导电的化合物都是电解质 |
| C.25℃时,0.1mol/L的盐酸中氢离子浓度大于0.1mol/L的醋酸中氢离子浓度 |
| D.BaSO4属于强电解质,所以其水溶液导电能力很强 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 >HSO3->
>HSO3-> ,水杨酸(
,水杨酸( )与亚硫酸钠溶液反应,可能生成的物质是
)与亚硫酸钠溶液反应,可能生成的物质是A. | B.SO2 | C.NaHSO3 | D. |
查看答案和解析>>
科目: 来源:不详 题型:填空题


查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.醋酸钠溶液显碱性 |
B.10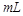  =2的醋酸溶液加水稀释到100 =2的醋酸溶液加水稀释到100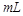   3 3 |
C.中和10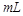 0.1 0.1 醋酸溶液,需要消耗0.1 醋酸溶液,需要消耗0.1 氢氧化钠溶液10 氢氧化钠溶液10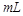 |
| D.0.1 mol·L-1的醋酸溶液中,氢离子浓度约为0.001 mol·L-1 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.pH由小到大的顺序是①< ②< ③< ④ |
| B.溶液中水电离出的H+浓度由小到大的顺序是②<①<④<③ |
| C.取一定体积的④溶液,分别和①、②、③溶液完全中和,消耗①、②、③溶液的体积由小到大的顺序是②<①<③ |
| D.取a体积的①溶液和b体积的④溶液混合后,溶液的pH为3,则a:b约为11:9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com