
科目: 来源:不详 题型:单选题
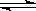 F—(aq) + H2O(l) △H=-67.7 kJ/mol
F—(aq) + H2O(l) △H=-67.7 kJ/mol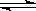 H2O(l) △H=-57.3kJ/mol
H2O(l) △H=-57.3kJ/mol| A.当氢氟酸溶液温度升高,HF的电离程度减小(不考虑挥发) |
B.水电离的热化学方程式为:H2O(1) 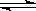 H+(aq)+OH—(aq);△H= +57.3kJ/mol H+(aq)+OH—(aq);△H= +57.3kJ/mol |
| C.当c > 0.1时,一定不存在:c(Na+) = c(F—) |
| D.若混合后溶液中:c(Na+)>c(OH—) >c(F—)>c(H+),则c一定小于0.1 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.0.1mol/L NaCl溶液 | B.0.1mol/L NH4Cl溶液 |
| C.0.1mol/L KOH溶液 | D.0.1mol/L KAlO2溶液 |
查看答案和解析>>
科目: 来源:不详 题型:计算题
 Ag2O2↓+2KNO3+K2SO4+2H2O
Ag2O2↓+2KNO3+K2SO4+2H2O查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.AgCl>AgI> Ag2CrO4 | B.Ag2CrO4>AgCl>AgI |
| C.AgCl> Ag2CrO4>AgI | D.Ag2CrO4>AgI>AgCl |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 2B(g);△H,若正反应的活化能为Ea kJ·mol-1,逆反应的活化能
2B(g);△H,若正反应的活化能为Ea kJ·mol-1,逆反应的活化能| A.全部 | B.③④⑤⑥ | C.②④⑤⑥ | D.①②④⑤ |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.红棕色的NO2气体加压后颜色先变深再变浅 |
| B.H2、I2、HI混合气体加压后颜色变深 |
| C.二氧化硫转化为三氧化硫时增加空气的量以提高二氧化硫的转化率 |
| D.打开汽水瓶,看到有大量的气泡逸出 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
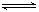 cC(g)+dD(g)达到平衡时,各物质的物质的量浓度满足以下关系:
cC(g)+dD(g)达到平衡时,各物质的物质的量浓度满足以下关系: (为一常数),K称为化学平衡常数,它的值只与温度有关。现有反应:CO(g)+H2O(g)
(为一常数),K称为化学平衡常数,它的值只与温度有关。现有反应:CO(g)+H2O(g)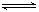 CO2(g)+H2(g),△H<0。在850℃时,K=1。
CO2(g)+H2(g),△H<0。在850℃时,K=1。查看答案和解析>>
科目: 来源:不详 题型:计算题
 2SO3△H<0
2SO3△H<0
查看答案和解析>>
科目: 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com