
科目: 来源:不详 题型:单选题
| A.pH为12的烧碱溶液与Ba(OH)2溶液的物质的量浓度之比 |
| B.K2S溶液中c(K+)与c(S2-)之比 |
| C.相同温度下0.2mol/L醋酸溶液与0.1mol/L醋酸溶液中的c(H+)之比 |
| D.10mL0.5mol/L的盐酸与5mL0.5mol/L的盐酸溶液中的c(H+)之比 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 的变化如下图所示。下列判断正确的是( )
的变化如下图所示。下列判断正确的是( ) 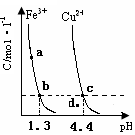
A.加适量浓NH3·H2O可使溶液由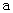 点变到 点变到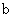 点 点 |
B.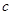  两点代表的溶液中 两点代表的溶液中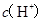 与 与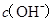 乘积不相等 乘积不相等 |
C.Cu(OH)2在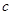 点比在d点代表的溶液中溶解程度小 点比在d点代表的溶液中溶解程度小 |
D.该温度下,氢氧化铁的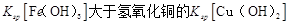 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.常温下,向含AgCl固体的AgCl溶液中加入NaCl固体,AgCl沉淀的量不变 |
| B.滴定终点时,溶液中CrO42-的浓度约为3.6×10-3 mol·L-1 |
| C.向10mL0.1moL/L AgNO3溶液中滴加3—5滴0.1moL/L NaCl溶液生成AgCl沉淀,再滴加KI溶液,生成AgI沉淀,能够说明Ksp(AgI)< Ksp(AgCl) |
| D.可用0.1 mol·L-1的KI溶液代替K2CrO4做指示剂 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
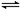 H++OH-;ΔH>0,下列叙述正确的是
H++OH-;ΔH>0,下列叙述正确的是| A.向水中加入稀醋酸,平衡逆移,c(H+)降低 |
| B.将水加热,KW增大,pH不变 |
| C.向水中加入少量固体硫酸氢钾,c(H+)增大,KW不变 |
| D.pH=10的NaOH溶液与pH=10的NaClO溶液中,水电离c(H+)之比等于106 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.0.1 mol·L-1的醋酸溶液中加水稀释,溶液中c(OH-)减小 |
| B.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) |
| C.pH=4的醋酸溶液与pH=10的烧碱溶液等体积混合后溶液呈酸性 |
| D.醋酸溶液中加入少量醋酸钾晶体,醋酸电离程度减小 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.饱和AgCl溶液与饱和Ag2CrO4溶液相比,前者的c(Ag+)大 |
| B.向氯化银的浊液中加入氯化钠溶液,氯化银的Ksp减小 |
| C.向0.0008 mol·L- 1的K2CrO4溶液中加入等体积的0.002 mol/L AgNO3 溶液,则CrO42-完全沉淀 |
| D.将0.001 mol·L- 1的AgNO3 溶液滴入0.001 mol·L- 1的KCl和0.001 mol·L- 1的K2CrO4溶液,则先产生AgCl沉淀 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.电解质的溶解开始后,只有电解质的溶解过程,没有电解质的析出过程 |
| B.沉淀溶解达到平衡时,沉淀的速率和溶解的速率相等 |
| C.沉淀溶解达到平衡时,溶液中溶质的各离子浓度相等,且保持不变 |
| D.沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.BaSO4可做钡餐而BaCO3不能是因为Ksp(BaSO4)<Ksp(BaCO3) |
| B.在制腈纶纤维的1 L溶液中含SO42-为1.0×10-3 mol,则加入0.01 mol BaCl2不能使SO42-完全沉淀 |
| C.在清理有关仪器的BaSO4沉淀时,常加入饱和Na2CO3溶液,使BaSO4转化为BaCO3再用酸处理 |
| D.用稀H2SO4洗涤BaSO4效果比用水好,BaCO3也能用此法处理 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com