
科目: 来源:不详 题型:单选题
| A.25°C时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大 |
| B.25°C时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大 |
| C.25°C时,Mg(OH)2固体在20mL0.01 mol·L-1氨水中的Ksp比在20mL0.01mol·L-1NH4Cl溶液中的Ksp小 |
| D.25°C时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2不可能转化为MgF2 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.用溶解度数据判断煮沸Mg(HCO3)2溶液得到的产物是Mg(OH)2而不是MgCO3 。 |
| B.用pH数据推测不同强酸弱碱盐在水溶液中水解程度的大小。 |
| C.用反应热数据的大小判断不同反应的反应速率的快慢。 |
| D.用平衡常数的大小判断化学反应可能进行的程度。 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
| 化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 溶度积 | 1.8×10-10 | 1.4×10- | 6.3×10-50 | 5.4×10-13 | 8.3×10-17 |
| A.五种物质在常温下溶解度最大的是Ag2SO4 |
| B.将氯化银溶解于水后,向其中加入Na2S,则可以生成黑色沉淀Ag2S |
| C.氯化银、溴化银和碘化银三种物质在常温下的溶解度随着氯、溴、碘的顺序增大 |
| D.沉淀溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.pH=7的溶液一定是中性溶液 |
| B.能自发进行的化学反应,不一定是△H<0、△S>0 |
| C.白色污染、绿色食品中的“白”“绿”均指相关物质的颜色 |
| D.Ksp不仅与难溶电解质的性质和温度有关,而且与溶液中的离子浓度有关 |
查看答案和解析>>
科目: 来源:不详 题型:计算题
 干净、干燥、称重.
干净、干燥、称重. 计算说明当充分反应
计算说明当充分反应 后铜片的质量为何值时,CH3COOAg的KSP=2.0×10-3可以得到证实.(
后铜片的质量为何值时,CH3COOAg的KSP=2.0×10-3可以得到证实.( =2.24,
=2.24,  =1.41)
=1.41)查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.向c(SO42-)=1.05×10-5mol/L的BaSO4溶液中加入BaSO4固体,c(SO42-)增大 |
| B.向该饱和溶液中加入Ba(NO3)2固体,则BaSO4的溶度积常数增大 |
| C.向该饱和溶液中加入Na2SO4固体,则该溶液中c(Ba2+)>c(SO42-) |
| D.向该饱和溶液中加入BaCl2固体,则该溶液中c(SO42-)减小 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
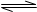 CH3COO-+H+,加水稀释后,溶液中所有离子浓度均减小;
CH3COO-+H+,加水稀释后,溶液中所有离子浓度均减小;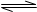 2Z(g)+W(s); △H>0平衡后,升高温度,该化学平衡正向移动;
2Z(g)+W(s); △H>0平衡后,升高温度,该化学平衡正向移动;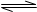 CH3COOH+OH-使得溶液中的c(OH-)>c(H+)
CH3COOH+OH-使得溶液中的c(OH-)>c(H+)| A.①②③④⑤ | B.②③④⑤⑥ | C.②③⑤⑥⑦ | D.①②⑤⑥⑦ |
查看答案和解析>>
科目: 来源:不详 题型:实验题
| A.两种难溶盐电解质,其中Ksp小的溶解度一定小 |
| B.向含有AgCl固体的溶液中加入适量的水使AgCl溶解又达到平衡时,AgCl的溶度积不变,其溶解度也不变 |
| C.将难溶电解质放入纯水中,溶解达到平衡时,电解质离子的浓度的乘积就是该物质的溶度积 |
| D.溶液中存在两种可以与同一沉淀剂生成沉淀的离子,则Ksp小的一定先生成沉淀 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
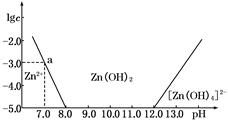
| c(HCl) | | | | | | | |
| (mol/L) | 0.50 | 1.00 | 2.04 | 2.90 | 4.02 | 5.16 | 5.78 |
| 103c(PbCl2) | | | | | | | |
| (mol/L) | 5.10 | 4.91 | 5.21 | 5.90 | 7.48 | 10.81 | 14.01 |
| A.随着盐酸浓度的增大,PbCl2固体的溶解度先变小后又变大 |
| B.PbCl2固体在0.50 mol/L盐酸中的溶解度小于在纯水中的溶解度 |
| C.PbCl2能与浓盐酸反应生成一种难电离的阴离子(络合离子) |
| D.PbCl2固体可溶于饱和食盐水 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 为难溶于水和酸的白色固体,
为难溶于水和酸的白色固体, 为难溶于水和酸是黑色固体。向
为难溶于水和酸是黑色固体。向 和水的悬浊液中加入足量的
和水的悬浊液中加入足量的 溶液并振荡,结果白色固体完全转化为黑色固体:
溶液并振荡,结果白色固体完全转化为黑色固体:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com