
科目: 来源:不详 题型:单选题
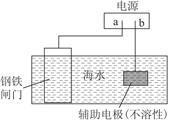
| A.图中所示是牺牲阳极的阴极保护法 |
| B.铁闸门作阴极,发生还原反应 |
| C.电子流向:a→铁闸门→辅助电极→b |
| D.辅助电极上的反应:O2+2H2O+4e-=4OH- |
查看答案和解析>>
科目: 来源:不详 题型:单选题
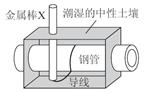
| A.金属棒X的材料可能为铜 |
| B.金属棒X的材料可能为钠 |
| C.钢管附近土壤的pH可能会上升 |
| D.这种方法称为外加电流的阴极保护法 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.电解AlCl3、FeCl3、CuCl2的混合溶液,在阴极上依次析出Cu、Fe、Al |
| B.电解CuSO4溶液一段时间后,加入适量Cu(OH)2可以使溶液恢复至原状态 |
| C.铅蓄电池在充电时,连接电源正极发生的电极反应为PbSO4+2e-=Pb+SO42- |
| D.将钢闸门与直流电流的负极相连,可防止钢闸门腐蚀 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
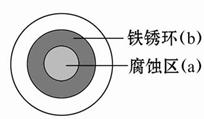
| A.液滴中的Cl-由a区向b区迁移 |
| B.液滴边缘是正极区,发生的电极反应为O2+2H2O+4e-=4OH- |
| C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH-形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
| D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为Cu-2e-=Cu2+ |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.我们使用的快餐杯表面有一层搪瓷,搪瓷层破损后仍能起到防止铁生锈的作用 |
| B.白铁(镀锌铁)镀层破损后,铁皮的腐蚀速率很慢 |
| C.轮船的船壳水线以下常装有一些锌块,这是利用了牺牲阴极的阳极保护法 |
| D.钢铁制造的暖气管道外常涂有一层沥青,这是钢铁的电化学保护法 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
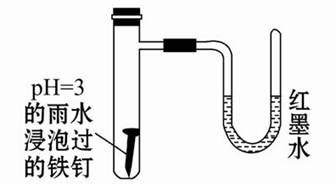
| A.开始时发生的是析氢腐蚀 |
| B.一段时间后发生的是吸氧腐蚀 |
| C.两种腐蚀负极的电极反应式均为Fe-2e-=Fe2+ |
| D.析氢腐蚀的总反应式为2Fe+O2+2H2O=2Fe(OH)2 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 |
| B.铅蓄电池放电时的负极和充电时的阳极均发生还原反应 |
| C.电解AlCl3、FeCl3、CuCl2的混合溶液时阴极上依次析出Cu、Fe、Al |
| D.电解食盐水一段时间后,可通入一定量的HCl气体来恢复原溶液 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.原电池是将化学能转化为电能的装置 |
| B.轮船底部镶嵌锌块,锌作负极,以防船体被腐蚀 |
| C.钢铁腐蚀的负极反应:Fe-3e-=Fe3+ |
| D.电镀时,镀层金属作阳极,镀件作阴极 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com