
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:问答题
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目: 来源:0107 月考题 题型:填空题
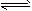 C(g)+D(g)过程中的能量变化如图所示,回答下列问题
C(g)+D(g)过程中的能量变化如图所示,回答下列问题
查看答案和解析>>
科目: 来源:期中题 题型:单选题
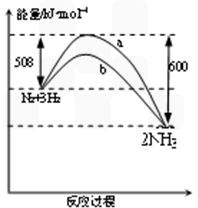
 2NH3(g) ΔH = 92kJ·mol-1
2NH3(g) ΔH = 92kJ·mol-1 查看答案和解析>>
科目: 来源:0118 同步题 题型:单选题
查看答案和解析>>
科目: 来源:0127 期末题 题型:单选题
[ ]
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.反应产物的总焓大于反应物的总焓时,反应吸热,△H<0 |
| B.生成物全部化学键形成时所释放的能量大于破坏反应物全部化学键所吸收的能量时,反应为吸热反应 |
| C.为了提高煤的利用率,常将煤直接燃烧 |
| D.在化学反应过程中,发生物质变化的同时伴随能量变化 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.化学反应过程中,分子的种类和数目一定发生改变 |
| B.如果某化学反应的△H和△S均小于0,则反应一定能自发进行 |
| C.化学反应过程中,一定有化学键的断裂和形成 |
| D.反应物的总焓大于反应产物的总焓时,△H>0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com