
科目: 来源:不详 题型:填空题

查看答案和解析>>
科目: 来源:不详 题型:填空题
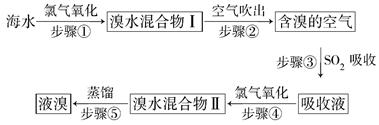
查看答案和解析>>
科目: 来源:不详 题型:填空题
| 华素片(西地碘片)使用说明书 【品名或组成】 品名:西地碘片 组成:华素片 英文名:Cydiodine Tablets 华素片(西地碘片)的主要活性成分是分子碘,含量1.5 mg/片。将碘利用分子分散技术制成分子态西地碘,并含适量薄荷脑等 【贮藏】 遮光、密闭、阴凉处保存 【有效期】 二年 |
查看答案和解析>>
科目: 来源:不详 题型:单选题

| A.各放一张质量相同的滤纸于天平的两托盘上,将NaOH固体放在左盘上称量 |
| B.欲除去NO中少量的NO2,将混合气体通入足量NaOH溶液 |
| C.实验室用图1所示装置制取少量氨气 |
| D.实验室用图2所示装置检验火柴头燃烧产生的SO2 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.Ba(OH)2、KSCN、NaCl、Mg(NO3)2(FeCl3溶液) |
| B.NaNO3、NaHCO3、(NH4)2SO3、Na2SiO3(H2SO4溶液) |
| C.NH4Br、K2CO3、NaI、CaCl2(AgNO3溶液) |
| D.(NH4)3PO4、NaBr、CuSO4、AlCl3(KOH溶液) |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.向某溶液中加稀盐酸,将产生的无色气体通入澄清石灰水中,石灰水变浑浊,则原溶液中一定有CO32-或HCO3- |
| B.向某溶液中加入硝酸钡溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,则原溶液中一定有SO42- |
| C.向某溶液中加入浓氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,则原溶液中存在NH4+ |
| D.向某溶液中加入硝酸银溶液产生白色沉淀,再加稀盐酸,沉淀不消失,则原溶液中一定有Cl- |
查看答案和解析>>
科目: 来源:不详 题型:填空题
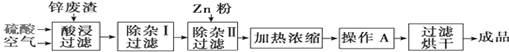
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 5.4 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 8.0 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
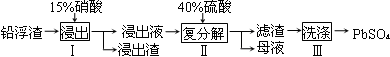
查看答案和解析>>
科目: 来源:不详 题型:单选题
| 选项 | 实验操作 | 现象 | 解释 |
| A. | 向某溶液中加入盐酸 | 产生无色气体 | 溶液中一定含有CO32? |
| B. | 新制Fe(OH)2露置于空气中一段时间 | 白色固体迅速变为灰绿色,最终变为红褐色 | 说明Fe(OH)2易被氧化成Fe(OH)3 |
| C. | 在CuSO4溶液中加入KI溶液,再加入苯,振荡 | 上层呈紫红色,下层有白色沉淀生产 | 铜离子可以氧化碘离子,白色沉淀可能为CuI |
| D. | 向某无色溶液中滴加硝酸酸化的BaCl2溶液 | 产生白色沉淀 | 溶液中一定含有SO42- |
查看答案和解析>>
科目: 来源:不详 题型:实验题
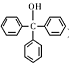 )是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的流程如图1所示,装置如图所示。
)是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的流程如图1所示,装置如图所示。

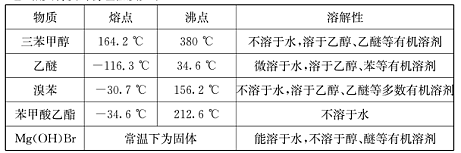
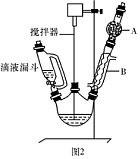

| A.水 | B.乙醚 | C.乙醇 | D.苯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com