
科目: 来源:不详 题型:单选题
| A.边滴定,边摇动溶液,溶液中首先析出AgSCN白色沉淀 |
| B.当Ag+定量沉淀后,少许过量的SCN-与Fe3+生成红色配合物,即为终点 |
| C.上述实验可用KCl标准溶液代替KSCN的标准溶液滴定Ag+ |
| D.滴定时,必须控制溶液一定的酸性,防止Fe3+水解,影响终点的观察 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:问答题

| 1 |
| 10 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
| 实验编号 | 待测血液的体积/mL | 滴入KMnO4溶液的体积/mL |
| 1 | 20.00 | 11.95 |
| 2 | 20.00 | 13.00 |
| 3 | 20.00 | 12.05 |
查看答案和解析>>
科目: 来源:不详 题型:多选题
A.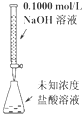 可以进行酸碱中和滴定实验 |
B.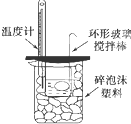 可以进行中和热的测定实验 |
C.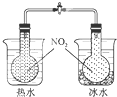 可验证温度对化学平衡的影响 |
D.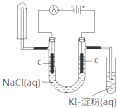 可检验食盐水通电后的部分产物 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
| 滴定次数 实验数据 | 1 | 2 | 3 | 4 | 5 |
| V(NaOH)/mL(初读数) | 0.00 | 0.20 | 0.00 | 0.10 | 0.05 |
| V(NaOH)/mL(终读数) | 15.75 | 15.20 | 14.98 | 15.12 | 15.05 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |

查看答案和解析>>
科目: 来源:不详 题型:问答题
| 实验编号 | 邻苯二甲酸氢钾的质量(g) | 待测NaOH溶液的体积(mL) |
| 1 | 0.4162 | 18.25 |
| 2 | 17.04 | |
| 3 | 16.96 |

查看答案和解析>>
科目: 来源:不详 题型:单选题
A.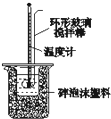 测定中和反应的反应热 |
B. 配制100mL 0.1mol/L盐酸 |
C.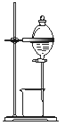 用来分离乙醇和水 |
D.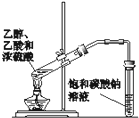 实验室制备乙酸乙酯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com