
科目: 来源:不详 题型:实验题
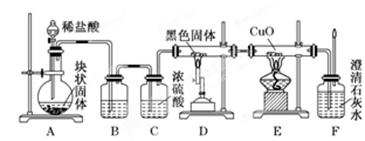
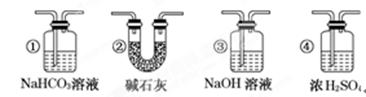
查看答案和解析>>
科目: 来源:不详 题型:实验题
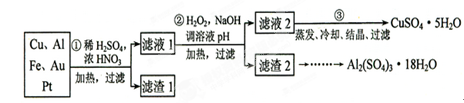
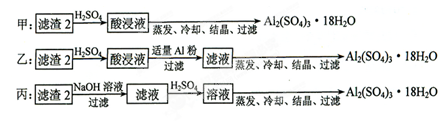
查看答案和解析>>
科目: 来源:不详 题型:实验题
查看答案和解析>>
科目: 来源:不详 题型:填空题
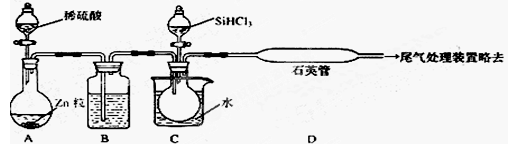
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.向氯化铁溶液中不断加入氢氧化钠溶液制备氢氧化铁胶体 |
| B.用铜粉和硫粉混合加热制备硫化铜 |
| C.用铁做阳极电解硫酸钠溶液可以制得氢氧化亚铁 |
| D.向铝盐溶液中不断滴入过量烧碱溶液制备Al(OH)3 |
查看答案和解析>>
科目: 来源:不详 题型:实验题
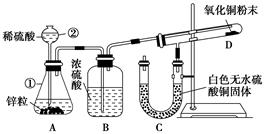
查看答案和解析>>
科目: 来源:不详 题型:实验题
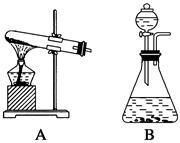
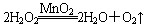 。反应中MnO2的作用是________。在实验室利用此反应制取氧气时,应选用的气体发生装置是________,简述检查本装置气密性的方法:______________________________________________。
。反应中MnO2的作用是________。在实验室利用此反应制取氧气时,应选用的气体发生装置是________,简述检查本装置气密性的方法:______________________________________________。查看答案和解析>>
科目: 来源:不详 题型:填空题
 (NH4)2S2O8+H2↑,
(NH4)2S2O8+H2↑, 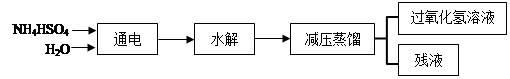
| A.不稳定性 | B.弱碱性 | C.氧化性 | D.还原性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com