
科目: 来源:不详 题型:实验题
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:实验题
| A.稀硫酸; | B.锌粒; | C.某溶液; | D.CaCO3固体;E、滴有紫色石蕊试液的蒸馏水;F、足量的澄清石灰水 |
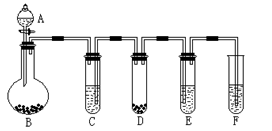
 装置D中:
装置D中:  装置F中:
装置F中: 查看答案和解析>>
科目: 来源:不详 题型:实验题
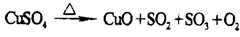
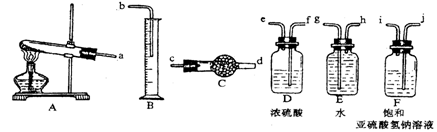
查看答案和解析>>
科目: 来源:不详 题型:实验题


查看答案和解析>>
科目: 来源:不详 题型:实验题
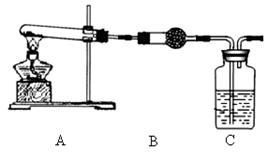
查看答案和解析>>
科目: 来源:不详 题型:单选题
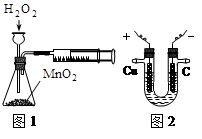
| A.利用右图1装置定量测定H2O2的分解速率 |
| B.利用右图2装置模拟工业上电解饱和食盐水 |
| C.配制FeCl3溶液时加入少量盐酸,以防止溶液浑浊 |
| D.用HNO2溶液做导电性实验,灯光较暗,说明HNO2是弱电解质 |
查看答案和解析>>
科目: 来源:不详 题型:实验题
 O2(g) = H2O(g) △H=-241.8 kJ·mol-1
O2(g) = H2O(g) △H=-241.8 kJ·mol-1查看答案和解析>>
科目: 来源:不详 题型:填空题
| A.用酸式滴定管取稀H2SO4 25.00mL,注入锥形瓶中,加入2滴酚酞。 |
| B.用待测定的溶液润洗酸式滴定管 |
| C.用蒸馏水洗干净滴定管 |
| D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2—3cm处,再把碱式滴定管固定好,调节液面至 刻度“0”或“0”刻度以下 |

查看答案和解析>>
科目: 来源:不详 题型:单选题
| 编号 | 实验内容 | 实验目的 |
| A | 将SO2通入酸性KMnO4溶液中 | 证明SO2具有氧化性 |
| B | 将Cl2通入NaBr溶液中 | 比较氯离子与溴离子的氧化性强弱 |
| C | 将铜与浓硝酸反应生成的气体收集后用冰水混合物冷却降温 | 研究温度对化学平衡的影响 |
| D | 分别向2支试管中加入相同体积不同浓度的H2O2溶液,再向其中1支加入少量MnO2 | 研究催化剂对H2O2分解速率的影响 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com