
科目: 来源:不详 题型:填空题
题号 | 实验要求 | 答案 |
(1) | 从碘水中提取碘单质 | |
(2) | 提纯混有少混NaCl的KNO3 | |
(3) | 鉴别NaCl和KCl | |
(4) | 测定某工业废水的酸碱度 | |
(5) | 检验自来水中残余氯分子 |

查看答案和解析>>
科目: 来源:不详 题型:实验题
 填序号)。
填序号)。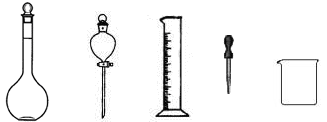
查看答案和解析>>
科目: 来源:不详 题型:实验题
 要的用途,分别是 和 ;
要的用途,分别是 和 ; 色。该同学还想通过实验分别证实溶质中含有Cu2+、SO42-,请你帮他想想办法,选择适当的试剂(写化学式),并写出其相应的离子方程式。
色。该同学还想通过实验分别证实溶质中含有Cu2+、SO42-,请你帮他想想办法,选择适当的试剂(写化学式),并写出其相应的离子方程式。| 溶质 | 加入试剂 | 离子方程式 |
| Cu2+ | | |
| SO42- | | |
 液浓度将
液浓度将  ;
;查看答案和解析>>
科目: 来源:不详 题型:填空题

 D.氢键 E.配位键 F.金属键 G.极性键
D.氢键 E.配位键 F.金属键 G.极性键
| | 熔点/℃ | 沸点/℃ | 溶解性 |
| 苯甲醛 | —26 | 179 | 微溶于水,易溶于乙醇、乙醚 |
| 苯甲酸 | 122 | 249 | 微溶于水,易溶于乙醇、乙醚 |
| 苯甲醇 | -15.3 | 205.0 | 稍溶于水,易溶于乙醇、乙醚 |
| 乙醚 | -116.2 | 34.5 | 微溶于水,易溶于乙醇 |
 萃取的效果 ▲ (填“好”或“差”)。
萃取的效果 ▲ (填“好”或“差”)。 馏装置,加热蒸馏并回收乙醚,应选择的加热方法是 ▲ (填字母代
馏装置,加热蒸馏并回收乙醚,应选择的加热方法是 ▲ (填字母代 号)。
号)。 冷却使结晶完全,抽滤,洗涤、干燥。抽滤完毕或中途停止抽滤时,应先 ▲ 。
冷却使结晶完全,抽滤,洗涤、干燥。抽滤完毕或中途停止抽滤时,应先 ▲ 。查看答案和解析>>
科目: 来源:不详 题型:实验题
查看答案和解析>>
科目: 来源:不详 题型:实验题
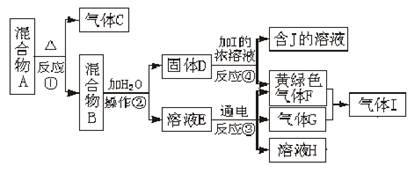
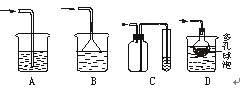
查看答案和解析>>
科目: 来源:不详 题型:实验题
 NaOH溶液吸收过量的CO2气体,至CO2
NaOH溶液吸收过量的CO2气体,至CO2 气体不再溶解;
气体不再溶解;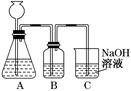
 的试剂是_____
的试剂是_____  _,作用是_____________________________________________
_,作用是_____________________________________________查看答案和解析>>
科目: 来源:不详 题型:实验题
 的实验并回答相关问题。
的实验并回答相关问题。 除尖嘴部分气泡后,使液面位于“0”刻度或“0”度以下。静置,读取数据并记录为NaOH标准溶液体积的初读数。
除尖嘴部分气泡后,使液面位于“0”刻度或“0”度以下。静置,读取数据并记录为NaOH标准溶液体积的初读数。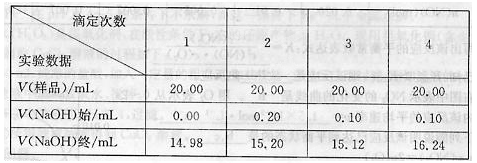
 要原因是 (填写序号)
要原因是 (填写序号) 吸取待测液
吸取待测液查看答案和解析>>
科目: 来源:不详 题型:实验题
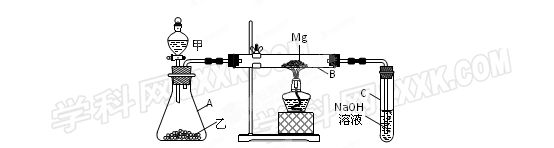 (1)选择制取SO2的最合适试剂 (填序号)。
(1)选择制取SO2的最合适试剂 (填序号)。
 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com