
科目: 来源:不详 题型:单选题
| A.加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉 |
| B.用萃取的方法分离汽油和煤油 |
| C.用溶解过滤的方法分离KNO3和NaCl固体的混合物 |
| D.将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
查看答案和解析>>
科目: 来源:不详 题型:实验题
 ⑥托盘天平。配制时,必须使用的仪器或用品有
⑥托盘天平。配制时,必须使用的仪器或用品有  (填序号),还缺少的仪器是 。
(填序号),还缺少的仪器是 。 高的是 (填序号)
高的是 (填序号) 时俯视刻度
时俯视刻度查看答案和解析>>
科目: 来源:不详 题型:单选题
A.向待检液中加入BaCl 2溶液有白色沉淀产生,再加盐酸,沉淀不消失,则原溶液中一定含有SO42- 2溶液有白色沉淀产生,再加盐酸,沉淀不消失,则原溶液中一定含有SO42- |
| B.向待检液中加入NaOH溶液并加热,有能使湿润的红色石蕊试纸变蓝的气体生成,则原溶液中一定含有NH4+ |
| C.向待检液中加入盐酸有能使澄清石灰水变浑浊的气体生成,则原溶液中一定含有大量的CO32- |
| D.向待检液中加入加入几滴氯水,再加入KSCN溶液,溶液立即变红,则原溶液中一定含有Fe3+ |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 ol·L-1的NaOH溶液,配制时:
ol·L-1的NaOH溶液,配制时: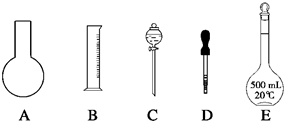
| A.加水定容时超过刻度线,又吸出少量水至刻度线 |
| B.忘记将洗涤液转入容量瓶 |
C.容量瓶洗涤后内壁有水珠而未作干燥处理 |
| D.溶液未冷却即转入容量瓶 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。 错误之处
错误之处 查看答案和解析>>
科目: 来源:不详 题型:实验题
 记下刻度。
记下刻度。 些实验
些实验 操作引起的 。
操作引起的 。| A.转移待测液至容量瓶时,未洗涤烧杯 |
| B.酸式滴定管用蒸馏水洗涤后,直接装盐酸 |
| C.滴定时,反应容器摇动太激烈,有少量待测液溅出 |
| D.滴定到终点时,滴定管尖嘴悬有液滴 |
查看答案和解析>>
科目: 来源:不详 题型:实验题
 现象对所配溶液的浓度有什么影响?(填“偏高”、“偏低”或“无影响”)
现象对所配溶液的浓度有什么影响?(填“偏高”、“偏低”或“无影响”)
查看答案和解析>>
科目: 来源:不详 题型:实验题
 。
。 。
。 进行干燥处理__________。
进行干燥处理__________。查看答案和解析>>
科目: 来源:不详 题型:填空题
 Cu2+、NH4+、K+、CO32-、SO42-等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如
Cu2+、NH4+、K+、CO32-、SO42-等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如 下图所示:
下图所示:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com