
科目: 来源:不详 题型:实验题
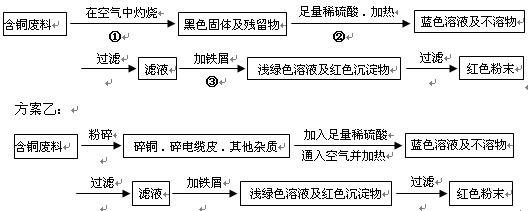
 __________________ _ __________
__________________ _ __________| 序号 | 实验操作 | 实验现象 | 结论及离子方程式 |
| ① | 取适量的样品于试管内 | —— | —— |
| ② | 用滴管滴入足量硫酸溶液,并充分振荡试管 | | |
| ③ | | 溶液先黄色,滴入KSCN溶液后显红色 | |
| | | | |
 师的建议完成上面操作步骤,获得晶体后对其进行检测
师的建议完成上面操作步骤,获得晶体后对其进行检测查看答案和解析>>
科目: 来源:不详 题型:实验题
 器.
器.查看答案和解析>>
科目: 来源:不详 题型:实验题
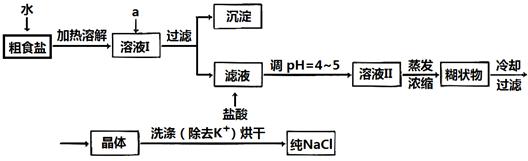
 器除天平、药匙、玻璃棒外还有___ _____(填仪器名称)。
器除天平、药匙、玻璃棒外还有___ _____(填仪器名称)。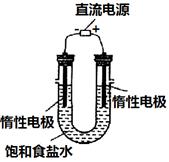
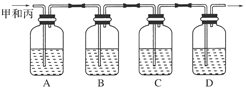
 MnCl2+Cl2↑+2H2O,据此,从下列所给仪器装置中选择制备并收集H2的装置_______(填代号)和制备并收集干燥、纯净Cl2的装置_________(填代号)。
MnCl2+Cl2↑+2H2O,据此,从下列所给仪器装置中选择制备并收集H2的装置_______(填代号)和制备并收集干燥、纯净Cl2的装置_________(填代号)。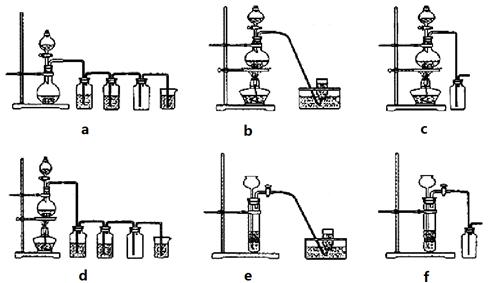
查看答案和解析>>
科目: 来源:不详 题型:实验题
 CO↑ + CO2↑ + H2O,
CO↑ + CO2↑ + H2O,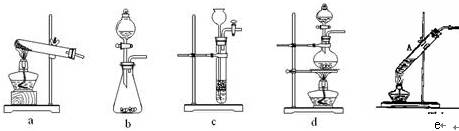
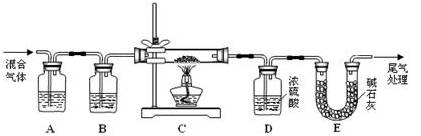
查看答案和解析>>
科目: 来源:不详 题型:实验题
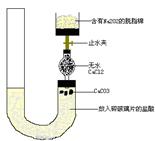
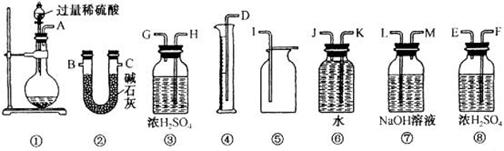
 的连接顺序 。
的连接顺序 。  。
。查看答案和解析>>
科目: 来源:不详 题型:单选题
 O4、 MgCl2四种固体的试剂是 ( )
O4、 MgCl2四种固体的试剂是 ( )| A.蒸馏水 | B.蒸馏水、硝酸 |
| C.蒸馏水、氨水 | D.蒸馏水、 BaC12溶液 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A | B | C | D |
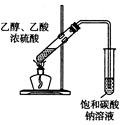 | 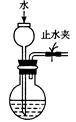 | 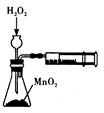 | 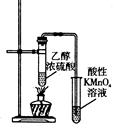 |
| 制取乙酸乙酯 | 检查装置的气密性 | 定量测定 H2O2的分解速率 | 证明 CH3CH2OH 发生消去反应生成了乙烯 |
查看答案和解析>>
科目: 来源:不详 题型:实验题
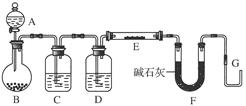
查看答案和解析>>
科目: 来源:不详 题型:实验题
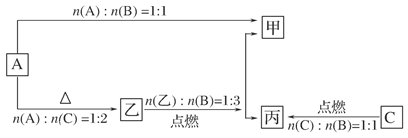
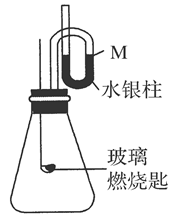
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com