
科目: 来源:不详 题型:填空题
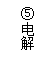
|
|
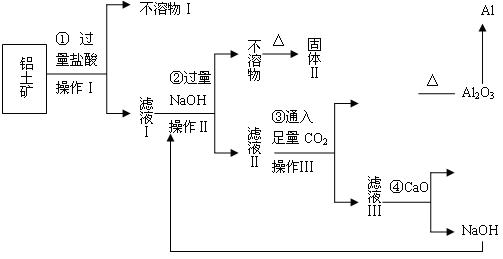
| A.复分解反应 | B.氧化还原反应 | C.置换反应 | D.分解反应 |
查看答案和解析>>
科目: 来源:不详 题型:实验题
 外活动小组设计实验探究氮的化合物的性质,装置如下图所示(A装置未画出),其中A为气体发生装置。A中所用试剂,从下列固体物质中选取:①NH4HCO3、②NH4Cl、③Ca(OH)2、④NaOH。
外活动小组设计实验探究氮的化合物的性质,装置如下图所示(A装置未画出),其中A为气体发生装置。A中所用试剂,从下列固体物质中选取:①NH4HCO3、②NH4Cl、③Ca(OH)2、④NaOH。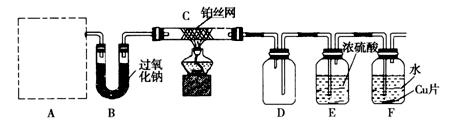
 __。
__。 ____________________________________________________________。
____________________________________________________________。查看答案和解析>>
科目: 来源:不详 题型:实验题

查看答案和解析>>
科目: 来源:不详 题型:实验题

 C
C 。
。| 实验次数 | 稀橙汁体积(mL) | 滴定用标准碘(水)溶液(mL) |
| 1 | 25.00 | 23.10 |
| 2 | 25.00 | 23.00 |
| 3 | 25.00 | 22.90 |
查看答案和解析>>
科目: 来源:不详 题型:实验题
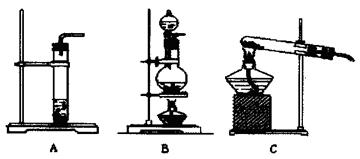
| 实验步骤 | 写出相应的离子方程式 |
| ①取试样加入足量10%的NaOH溶液,充分振荡后再将反应混合物倒入蒸馏烧瓶中蒸馏得到乙醇、水的混合物和产品A | ①OH-+C6H5-OH→C6H5O-+H2O ② |
| ②向步骤①的馏分中加入足量的生石灰,再次蒸馏浓缩,蒸气冷凝后得乙醇。 | CaO+H2O=Ca(OH)2 |
| ③向产品A中通入足量CO2,静置后分液得 和溶液B。 | |
| ④再向溶液B中加入足量 、静置、过滤后可得苯甲酸。 | |
查看答案和解析>>
科目: 来源:不详 题型:实验题
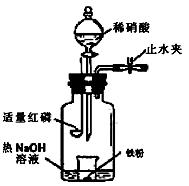
查看答案和解析>>
科目: 来源:不详 题型:填空题
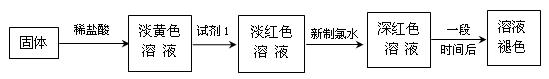
| 编 号 | 猜 想 |
| 甲 | 溶液中的+3价Fe又被还原为+2价Fe |
| 乙 | 溶液中的SCN-被过量的氯水氧化 |
| 丙 | 新制的氯水具有漂白性,将该溶液漂白 |
| 丁 | ? |
| 实验操作 | 预期现象 | 结 论 |
| | | 说明乙同学的猜想是合理的 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
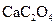 为白色沉淀物质)。首先取200g茶叶样品焙烧得灰粉后进行如下操作:
为白色沉淀物质)。首先取200g茶叶样品焙烧得灰粉后进行如下操作: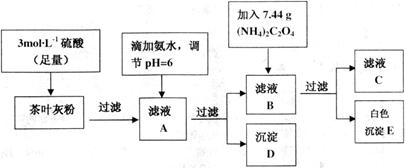
| 离子 | 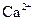 | 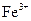 |
| 完全沉淀时的pH | 13 | 4.1 |
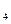 标准溶液滴定C溶液时所发生的反应为:
标准溶液滴定C溶液时所发生的反应为: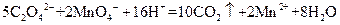 。
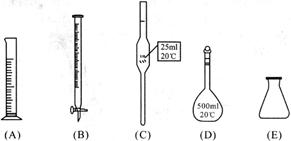
。
查看答案和解析>>
科目: 来源:不详 题型:填空题
 假设三: ;
假设三: ;
| | B装置的质量(g) | C装置的质量(g) | D装置的质量(g) |
| 实验前 | 15.4 | 262.1 | 223.8 |
| 试验后 | 6.1 | 264.8 | 230.4 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
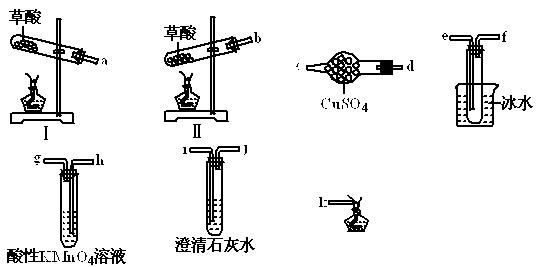
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com