
科目: 来源:不详 题型:单选题
| A.a>b | B.a=b | C.a<b | D.无法确定 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
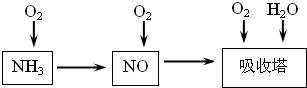
| ||
| 高温高压 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| 1 |
| 2 |
| A.+80.5 kJ/mol | B.+30.0 kJ/mol |
| C.-30.0 kJ/mol | D.-80.5 kJ/mol |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| 13 |
| 2 |
| 13 |
| 2 |
| 9 |
| 2 |
| 9 |
| 2 |
| A.-2878 kJ/mol | B.-2 658kJ/mol |
| C.-1746 kJ/mol | D.-1526 kJ/mol |
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.不管反应是一步完成还是分几步完成,其反应热相同 |
| B.反应热只与反应体系的始态和终态有关,而与反应的途径无关 |
| C.有些反应的反应热不能直接测得,可通过盖斯定律间接计算得到 |
| D.根据盖斯定律,热化学方程式中△H直接相加即可得总反应热 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.白磷在氧气中燃烧的热化学方程式是:P4(s)+5O2(g)=P4O10(s)△H=-745.8kJ?mol-1 |
| B.红磷转化成白磷时放出热量 |
| C.红磷比白磷稳定 |
| D.31g红磷中蕴含的能量为738.5kJ |
查看答案和解析>>
科目: 来源:天津 题型:问答题
| 高温 |
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成份 | WO3 W2O5 WO2 W |
| ||
| 约3000℃ |
查看答案和解析>>
科目: 来源:同步题 题型:单选题
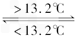 Sn(s,白) ΔH3=+2.1 kJ/mol
Sn(s,白) ΔH3=+2.1 kJ/mol 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com