
科目: 来源:不详 题型:单选题
| A.煤的气化是化学变化,煤的液化是物理变化 |
| B.甲烷是一种清洁燃料,可用作燃料电池的燃料 |
| C.蔗糖与淀粉水解的最终产物都是葡萄糖 |
| D.石油分馏可以得到乙烯、丙烯、甲烷等化工原料 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
A.2NaCl(熔融) 2Na+Cl2↑ 2Na+Cl2↑ | B.MgO+C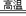 Mg+CO↑ Mg+CO↑ |
C.Al2O3+3CO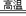 2Al+3CO2 2Al+3CO2 | D.2HgO 2Hg+O2↑ 2Hg+O2↑ |
查看答案和解析>>
科目: 来源:不详 题型:单选题
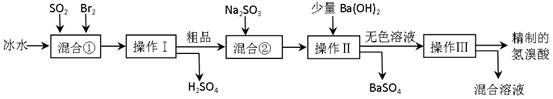
| A.正确操作步骤的顺序是⑤②③①④ |
| B.步骤④电解时阴极产生氯气 |
| C.直接在空气中将MgCl2溶液蒸干可得到Mg(OH)2高网 |
| D.此法提取镁的过程中涉及置换、分解、化合和复分解反应资 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
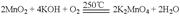 ;
;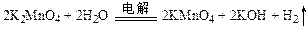 。
。| A.上述物质中,氧化性:KMnO4> K2MnO4 >O2 |
| B.上述过程中,每生成1 mol KMnO4需转移6 mol 电子 |
| C.电解时,KMnO4在阳极区生成 |
| D.电解时,阴极周围pH减小 |
查看答案和解析>>
科目: 来源:不详 题型:填空题

 (1)合成氨反应反应N2(g)+3H2(g)
(1)合成氨反应反应N2(g)+3H2(g)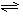 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);使用催化剂 反应的ΔH(填“增大”“减小”或“不改变”)。
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);使用催化剂 反应的ΔH(填“增大”“减小”或“不改变”)。 (2)已知:N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-543kJ·mol-1
(2)已知:N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-543kJ·mol-1
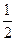 H2(g)+
H2(g)+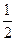 F2(g)=HF(g);△H=-269kJ·mol-1
F2(g)=HF(g);△H=-269kJ·mol-1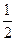 O2(g)=H2O(g);△H=-242kJ·mol-1
O2(g)=H2O(g);△H=-242kJ·mol-1 则反应 N2H4(g)+2F2(g)=N2(g)+4HF(g)的
则反应 N2H4(g)+2F2(g)=N2(g)+4HF(g)的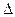 H="_____________" kJ·mol-1。
H="_____________" kJ·mol-1。 (3)已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20。在25℃下,向浓度均为0.1 mol·L-1的MgCL2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为______。
(3)已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20。在25℃下,向浓度均为0.1 mol·L-1的MgCL2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为______。 (4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”);用含a的代数式表示此时溶液中NH3·H2O的物质的量浓度__________ mol·L-1。(说明:溶液的体积可以直接相加)
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”);用含a的代数式表示此时溶液中NH3·H2O的物质的量浓度__________ mol·L-1。(说明:溶液的体积可以直接相加)查看答案和解析>>
科目: 来源:不详 题型:填空题
 科学院宣布,将2007年诺贝尔化学奖授予德国马普学会弗里茨-哈伯(Fritz-Haber)研究所的格哈德·埃特尔(Gerhard Ertl)教授,以表彰他在固体表面化学过程研究领域作出的开拓性成就。合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3。
科学院宣布,将2007年诺贝尔化学奖授予德国马普学会弗里茨-哈伯(Fritz-Haber)研究所的格哈德·埃特尔(Gerhard Ertl)教授,以表彰他在固体表面化学过程研究领域作出的开拓性成就。合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3。 =4FeO +CO2↑,为制得这种催化活性最高的催化剂,应向480g Fe2O3粉末中加入碳粉的质量为_________ g。
=4FeO +CO2↑,为制得这种催化活性最高的催化剂,应向480g Fe2O3粉末中加入碳粉的质量为_________ g。查看答案和解析>>
科目: 来源:不详 题型:填空题
 2NH3(g) △H=" -92.4KJ/mol " ,据此回答以下问题:
2NH3(g) △H=" -92.4KJ/mol " ,据此回答以下问题: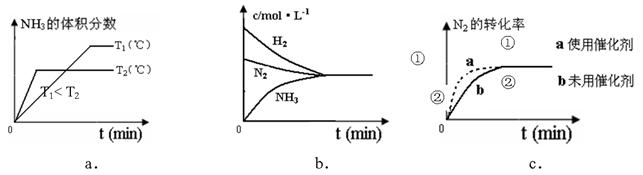
查看答案和解析>>
科目: 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com