
科目: 来源:不详 题型:判断题
查看答案和解析>>
科目: 来源:不详 题型:判断题
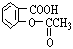 若将阿司匹灵溶于过量的氢氧化钠溶液,其反应的化学方程式为:_________________________
若将阿司匹灵溶于过量的氢氧化钠溶液,其反应的化学方程式为:_________________________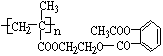
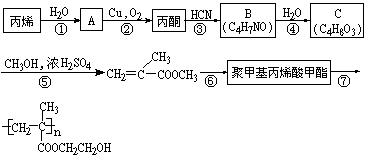
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.CO在铂表面被氧化生成CO2 | B.汽车尾气中NOx在铂表面反应转化为N2 |
| C.CO在铂表面可与O2、NOx反应 | D.铂在反应中起氧化作用 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.这些金属的化合物熔点低 | B.它们都是轻金属 | C.它们的性质很活泼 | D.此方法成本低 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.5 | B.6 | C.7 | D.8 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.该灰黑色粉末作抗氧化剂 |
| B.该灰黑色粉末不可食用 |
| C.小袋中原来装有铁粉 |
| D.小袋中原来装有Fe2O3 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
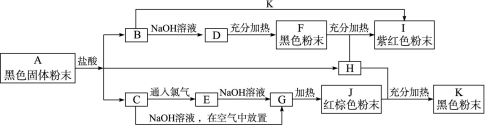
查看答案和解析>>
科目: 来源:不详 题型:实验题
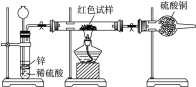
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.铁粉中混有锌粉杂质(稀硫酸) |
| B.FeCl3中混有FeCl2杂质(Cl2) |
| C.CO气体中混有CO2杂质(NaOH溶液) |
| D.SiO2中混有CaCO3杂质(盐酸) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com