
科目: 来源:不详 题型:单选题
 Z(g),经60s达到平衡生成0.3mol的Z,下列说法正确的是( )
Z(g),经60s达到平衡生成0.3mol的Z,下列说法正确的是( )| A.60 s时Z的平衡浓度为O.03mol/L |
| B.将容器容积变为20 L,Z的新平衡浓度将等于原平衡浓度的一半 |
| C.若温度和体积不变,往容器内增加1 mol Y,Y的转化率将增大 |
| D.若升高温度,X的体积分数增大,则正反应的△H>O |
查看答案和解析>>
科目: 来源:不详 题型:单选题

A.c0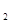 (g)+H (g)+H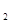 (g) (g)  F=e=CO(g)+H F=e=CO(g)+H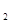 0(g)△H>0 0(g)△H>0 |
B.CH CH CH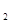 0H(g) 0H(g)  CH CH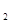 =CH =CH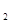 (g)+H (g)+H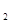 0(g)△H>0 0(g)△H>0 |
C.2C H H CH CH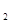 CH CH (g)+0 (g)+0 (g) (g)  2C 2C H H CH=CH CH=CH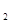 (g)+2H (g)+2H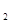 O(g)△H<0 O(g)△H<0 |
D.C0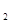 (g)+2NH (g)+2NH (g) (g)  CO(NH CO(NH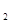 ) )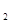 (s)+H (s)+H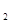 0(g)△H<0 0(g)△H<0 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 容包括:化学平衡、电离平衡、水解平衡和
容包括:化学平衡、电离平衡、水解平衡和 4C(g) △H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)
4C(g) △H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c) (g)
(g)  2CO(g)平衡常数K的表达式为 ;
2CO(g)平衡常数K的表达式为 ; 0(g)t
0(g)t CO(g)+H
CO(g)+H (g)的平衡常数为K1;H
(g)的平衡常数为K1;H (g)+CO
(g)+CO (g)
(g)  C0(g)
C0(g) 0(g)的平衡常数为恐,则K
0(g)的平衡常数为恐,则K 与K
与K 、K
、K 二者的关系为 。
二者的关系为 。 +0
+0
 2S0
2S0 的平衡常数K=19。在该温度下的体积
的平衡常数K=19。在该温度下的体积 )=lmol·L
)=lmol·L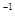 c0(O
c0(O )=1mol·L
)=1mol·L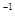 ,当反应在该温度下SO
,当反应在该温度下SO 转化率
转化率
 cC(g)+riD(g)△H=
cC(g)+riD(g)△H= kJ·mol
kJ·mol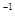 ;若
;若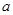 +b>
+b> 0(填“>”或“<”)。
0(填“>”或“<”)。查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.反应2A(g) + B(g) =" 3C" (s) + D(g)在一定条件下能自发进行,说明该反应的ΔH<0 |
| B.常温下,将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| C.常温下,H2CO3分子不可能存在于pH=8的碱性溶液中 |
| D.在合成氨工业中,移走NH3可增大正反应速率,提高原料转化率 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 VO2++ 2H++V2+。
VO2++ 2H++V2+。 N2(g)+2CO2(g);△H<0。
N2(g)+2CO2(g);△H<0。
查看答案和解析>>
科目: 来源:不详 题型:填空题
 2NH3(g);△H<0 。
2NH3(g);△H<0 。
查看答案和解析>>
科目: 来源:不详 题型:填空题
 2SO3(g);
2SO3(g);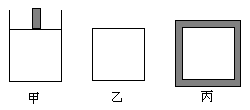
查看答案和解析>>
科目: 来源:不详 题型:单选题
 Z反应影响的示意图,下列叙述正确的是
Z反应影响的示意图,下列叙述正确的是
| A.X和Y中只有一种为气态,z为气态 |
| B.X、Y、Z均为气态 |
| C.上述可逆反应的正反应为放热反应 |
| D.上述反应的逆反应的△H>0 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 N的键能是946 kJ/mol,H—H的键能为436 kJ/mol,N—H的键能为391 kJ/mol,请据此写出合成氨反应的热化学方程式 ;
N的键能是946 kJ/mol,H—H的键能为436 kJ/mol,N—H的键能为391 kJ/mol,请据此写出合成氨反应的热化学方程式 ;查看答案和解析>>
科目: 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com