
科目: 来源:不详 题型:填空题
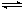 2NH3,达平衡后,测得反应放出的热量为18.4 kJ,混合气体总的物质的量为3.6 mol,容器内的压强变为原来的90%。又知N2和H2的转化率相同。
2NH3,达平衡后,测得反应放出的热量为18.4 kJ,混合气体总的物质的量为3.6 mol,容器内的压强变为原来的90%。又知N2和H2的转化率相同。 。
。 述平衡完全相同。
述平衡完全相同。查看答案和解析>>
科目: 来源:不详 题型:单选题
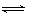 pC(g)+qD(g)△H 的下列4个图象中,图象及对应解读均正确的是( )
pC(g)+qD(g)△H 的下列4个图象中,图象及对应解读均正确的是( )
| A.图①表示反应从正反应开始,m+n>p+q |
| B.图②表示反应从逆反应开始,△H>0 |
| C.图③表示反应从逆反应开始,△H>0 |
| D.图④表示反应从正反应开始,有无催化剂参与反应的比较 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
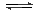 2NH3(g) ΔH = -46.19 kJ. mol—1,关于这个反应的平衡常数K,下列说法正确的是( )
2NH3(g) ΔH = -46.19 kJ. mol—1,关于这个反应的平衡常数K,下列说法正确的是( )| A.随温度升高K增加 | B.随压强升高K增加 |
| C.随温度升高K减小 | D.随压强升高K减小 |
查看答案和解析>>
科目: 来源:不详 题型:填空题

查看答案和解析>>
科目: 来源:不详 题型:填空题
 2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:
2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol·L—1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
| | N2 | H2 | NH3 |
| 起始浓度(mol/L) | 0.2 | 0.3 | 0.2 |
| 平衡浓度(mol/L) | a | b | c |
 4NH3(g)+3O2(g),此反应的△S__________0(填“
4NH3(g)+3O2(g),此反应的△S__________0(填“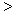 ”、 “
”、 “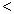 ”或“=”), △H=_____________。
”或“=”), △H=_____________。查看答案和解析>>
科目: 来源:不详 题型:填空题
 4NO(g)+6H2O (g)+1025 kJ
4NO(g)+6H2O (g)+1025 kJ 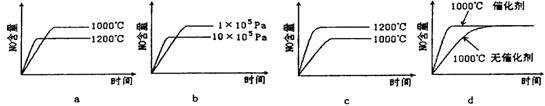
| 时间/浓度 | c(NH3)(mol/L) | C(O2)(mol/L) | C(NO)(mol/L) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.8 | 1.6 | 0.5 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.正反应速率一定增大 | B.生成物的质量分数一定增大 |
| C.逆反应速率一定减小 | D.至少有一种反应物的转化率增大 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
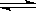 CH3COO-+H+
CH3COO-+H+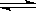 CH3COOH+OH-
CH3COOH+OH- 3COO-),则溶液的pH为_______
3COO-),则溶液的pH为_______ (填数值)。
(填数值)。查看答案和解析>>
科目: 来源:不详 题型:单选题
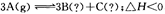 ,下列分析一定正确的是
,下列分析一定正确的是查看答案和解析>>
科目: 来源:不详 题型:填空题
 N2(g)+ 3 H2(g)。其中物质H2的物质的量变化如下图所示。
N2(g)+ 3 H2(g)。其中物质H2的物质的量变化如下图所示。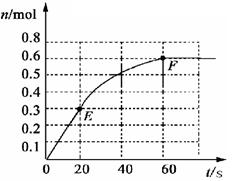

 d.再充入N2
d.再充入N2查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com