
科目: 来源:不详 题型:单选题
A.C(s) + CO2(g) 2CO(g) (正反应为吸热反应) 2CO(g) (正反应为吸热反应) |
B.3O2(g) 2O3(g)(正反应为吸热反应) 2O3(g)(正反应为吸热反应) |
C.CO(g) + NO2(g) CO2(g)+NO(g) (正反应为放热反应) CO2(g)+NO(g) (正反应为放热反应) |
D.N2 (g) + 3H2(g) 2NH3(g) (正反应为放热反应) 2NH3(g) (正反应为放热反应) |
查看答案和解析>>
科目: 来源:不详 题型:单选题
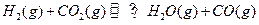 的平衡常数
的平衡常数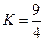 .该温度下在甲、乙、丙三个恒容密闭容器中,
.该温度下在甲、乙、丙三个恒容密闭容器中,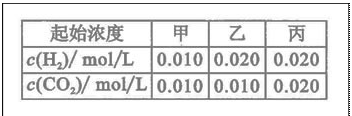
查看答案和解析>>
科目: 来源:不详 题型:填空题
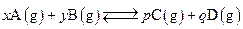
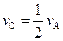 ;反应2min时,A的浓度减少了
;反应2min时,A的浓度减少了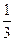 ,B的物质的量减少了
,B的物质的量减少了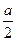 mol,有amolD生成。
mol,有amolD生成。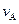 =,
=,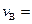 ;
;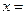 、
、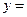 、
、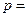 、
、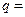 ;
;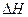
查看答案和解析>>
科目: 来源:不详 题型:填空题
 B(OCH3)3 +3H2O中,H3BO 3的转化率(
B(OCH3)3 +3H2O中,H3BO 3的转化率(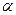 )在不同温度下随反应时间(t)的变化见图12,由此图可得出:
)在不同温度下随反应时间(t)的变化见图12,由此图可得出: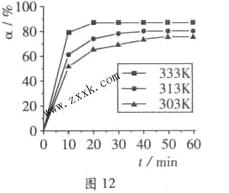
 _____0(填“<”、“=”或“>”).
_____0(填“<”、“=”或“>”). [B(O
[B(O H)4]-( aq)+H+(aq)已知0.70 mol·L-1 H3BO 3溶液中,上述反应于298K达到平衡时,c平衡(H+)="2." 0 × 10-5mol·L-1,c平衡(H3BO 3)≈c起始(H3BO 3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)
H)4]-( aq)+H+(aq)已知0.70 mol·L-1 H3BO 3溶液中,上述反应于298K达到平衡时,c平衡(H+)="2." 0 × 10-5mol·L-1,c平衡(H3BO 3)≈c起始(H3BO 3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)查看答案和解析>>
科目: 来源:不详 题型:单选题
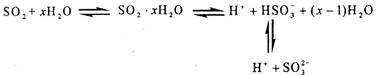
| A.该溶液中存在着SO2分子 |
| B.该溶液中H+浓度是SO2- 3浓度的2倍 |
| C.向该溶液中加入足量的酸都能放出SO2气体 |
| D.向该溶液中加入过量NaOH可得到Na2SO3 、NaHSO3和NaOH的混合溶液 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 2HI (g)达平衡的是
2HI (g)达平衡的是| A.单位时间内消耗amol H2,同时消耗 2amol HI |
| B.容器内的总压强不随时间变化 |
| C.容器内H2、I2不再减少,HI不再增加 |
| D.单位时间内每生成amol HI,同时a NA个HI分子分解 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 F(g)+xG(g);△H<0。若起始时E浓度为a mol·L-1,F、G浓度均为0,达平衡时E浓度为0.5a mol·L-1;若E的起始浓度改为 2a mol·L-1,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是
F(g)+xG(g);△H<0。若起始时E浓度为a mol·L-1,F、G浓度均为0,达平衡时E浓度为0.5a mol·L-1;若E的起始浓度改为 2a mol·L-1,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是 | A.升高温度时,正反应速率加快、逆反应速率减慢 |
| B.若x=l,容器体积保持不变,新平衡下E的体积分数为50% |
| C.若x=2,容器体积保持不变,新平衡下F的平衡浓度大于0.5a mol·L-1 |
| D.若x=2,容器压强保持不变,新平衡下E的物质的量为a mol |
查看答案和解析>>
科目: 来源:不详 题型:实验题
 I3-。通过测平衡体系中c(I2)、c(I-)和c(I3-),就可求得该反应的平衡常数。
I3-。通过测平衡体系中c(I2)、c(I-)和c(I3-),就可求得该反应的平衡常数。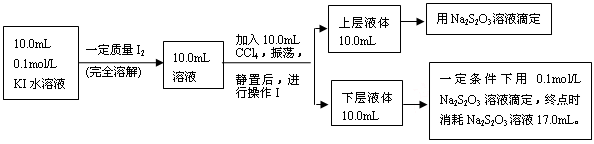
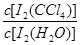 是一个常数(用Kd表示,称为分配系数),且室温条件下Kd=85。回答下列问题:
是一个常数(用Kd表示,称为分配系数),且室温条件下Kd=85。回答下列问题: I3-的平衡常数K=__________(用具体数据列出计算式即可)。)
I3-的平衡常数K=__________(用具体数据列出计算式即可)。)查看答案和解析>>
科目: 来源:不详 题型:单选题
 2SO3(g);ΔH<0.下列结论中正确的是
2SO3(g);ΔH<0.下列结论中正确的是| A.若温度不变,将容器的体积增大一倍,此时的SO2浓度变为原来的0.48倍 |
| B.若平衡时SO2、O2的转化率相等,说明反应开始时,两者的物质的量之比为2:1 |
| C.若从平衡体系中分离出SO3,则有利于提高SO2的转化率和加快正反应速率 |
| D.平衡状态时SO2、O2、SO3的物质的量之比一定为2:1:2 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
 3C(气), 在一定的条件下, 使一定量A和B气体反应, 达到平衡状态时, 具有的性质是( )
3C(气), 在一定的条件下, 使一定量A和B气体反应, 达到平衡状态时, 具有的性质是( )| A.各物质的浓度之比为 [A] : [B] : [C] =" 2" : 3 : 3 |
| B.平衡时气体的总体积是反应开始时的 3/5 |
| C.平衡混合物中各组份的浓度相等 |
| D.单位时间内, 若消耗了 a mol A 物质, 同时也消耗了 1.5 a mol 的C物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com