
科目: 来源:2014年高考化学考前题型专练 保温训练(二)(解析版) 题型:选择题
某化学学习小组学习电化学后,设计了下面的实验装置图:

下列有关该装置图的说法中正确的是 ( )。
A.合上电键后,盐桥中的阳离子向甲池移动
B.合上电键后,丙池为电镀银的电镀池
C.合上电键后一段时间,丙池中溶液的pH增大
D.合上电键后一段时间,当丙池中生成标准状况下560 mL气体时,丁池中理论上最多产生2.9 g固体
查看答案和解析>>
科目: 来源:2014年高考化学考前题型专练 保温训练(二)(解析版) 题型:选择题
下列与化学反应能量变化相关的叙述正确的是 ( )。
A.应用盖斯定律,可计算某些难以直接测量的反应焓变
B.1 mol S完全燃烧放热297.3 kJ,其热化学方程式:S+O2=SO2 ΔH=-297.3 kJ·mol-1
C.1 mol H2SO4与1 mol Ba(OH)2反应生成1 mol BaSO4沉淀时放出的热量叫做中和热
D.反应热的大小与反应物所具有的能量和生成物所具有的能量无关
查看答案和解析>>
科目: 来源:2014年高考化学考前题型专练 保温训练(二)(解析版) 题型:选择题
下列实验操作中,主要不是从安全因素考虑的是 ( )。
A.用NH4Cl、Ca(OH)2制备NH3时,可用如图所示装置吸收尾气
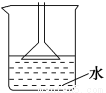
B.制备Fe(OH)2时,吸有NaOH溶液的胶头滴管要插入亚铁盐溶液中再挤出NaOH溶液
C.加热试管中的固体时,试管口应略向下倾斜
D.用氢气还原氧化铜时,先通一会氢气,再加热氧化铜
查看答案和解析>>
科目: 来源:2014年高考化学考前题型专练 保温训练(二)(解析版) 题型:选择题
已知一定温度下,有下列难溶电解质的溶解平衡数据:
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
Ksp/25 ℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
则对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不正确的是 ( )。
A.向该混合溶液中加过量铁粉,能观察到红色固体析出
B.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
C.该混合溶液中c(SO42-)∶[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5∶4
D.向该混合溶液中加入适量氯水,并调节pH至3~4后过滤,能得到纯净的CuSO4溶液
查看答案和解析>>
科目: 来源:2014年高考化学考前题型专练 保温训练(二)(解析版) 题型:填空题
党的十八大报告中首次提出“美丽中国”的宏伟目标。节能减排是中国转型发展的必经之路,工业生产中联合生产是实现节能减排的重要措施,下图是几种工业生产的联合生产工艺:
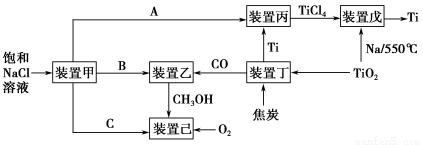
请回答下列问题:
(1)装置甲为电解池,根据图示转化关系可知:A为____________(填化学式),阴极反应式为____________。
(2)装置丙的反应物为Ti,而装置戊的生成物为Ti,这两个装置在该联合生产中并不矛盾,原因是_________________________________________________
装置戊进行反应时需要的环境为________(填字母序号)。
A.HCl气体氛围中 B.空气氛围中 C.氩气氛围中 D.水中
(3)装置乙中发生的是工业合成甲醇的反应:CO(g)+2H2(g)??CH3OH(g) ΔH<0。
①该反应在不同温度下的化学平衡常数(K)如下表:
温度/℃ | 250 | 350 |
K | 2.041 | x |
符合表中的平衡常数x的数值是________(填字母序号)。
A.0 B.0.012 C.32.081 D.100
②若装置乙为容积固定的密闭容器,不同时间段各物质的浓度如下表:
| c(CO) | c(H2) | c(CH3OH) |
0 min | 0.8 mol·L-1 | 1.6 mol·L-1 | 0 |
2 min | 0.6 mol·L-1 | y | 0.2 mol·L-1 |
4 min | 0.3 mol·L-1 | 0.6 mol·L-1 | 0.5 mol·L-1 |
6 min | 0.3 mol·L-1 | 0.6 mol·L-1 | 0.5 mol·L-1 |
反应从2 min到4 min之间,H2的平均反应速率为________。反应达到平衡时CO的转化率为________。反应在第2 min时改变了反应条件,改变的条件可能是________(填字母序号)。
A.使用催化剂 B.降低温度
C.增加H2的浓度
(4)装置己可以看作燃料电池,该燃料电池的负极反应式为____________ ________________________________________________。
查看答案和解析>>
科目: 来源:2014年高考化学考前题型专练 保温训练(二)(解析版) 题型:填空题
已知:H2A的A2-可表示S2-、SO42—、SO32—、SiO32—或CO32—。
(1)常温下,向20 mL 0.2 mol·L-1 H2A溶液中滴加0.2 mol·L-1 NaOH溶液。有关微粒物质的量变化如下图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)。请根据图示填空:
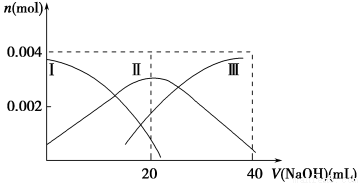
①当V(NaOH)=20 mL时,溶液中离子浓度大小关系:________。
②等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水________(填“大”、“小”或“相等”),欲使NaHA溶液呈中性,可以向其中加入_______________________________________________________。
(2)有关H2A的钠盐的热化学方程式如下:
①Na2SO4(s)=Na2S(s)+2O2(g) ΔH1=+1 011.0 kJ·mol-1
②2C(s)+O2(g)=2CO(g) ΔH2=-221.0 kJ·mol-1
则反应③Na2SO4(s)+4C(s)=Na2S(s)+4CO(g) ΔH3=________ kJ·mol-1。工业上制备Na2S时往往还要加入过量的碳,同时还要通入空气,目的有两个,其一是利用碳与氧气反应放出的热,维持反应③所需温度;其二是________________________________________。
(3)若H2A为硫酸:t ℃时,pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数KW=________。
查看答案和解析>>
科目: 来源:2014年高考化学考前题型专练 保温训练(二)(解析版) 题型:填空题
[物质结构与性质]已知:A、B、C、D、E、F六种元素,原子序数依次增大。A原子核外有两种形状的电子云,两种形状的电子云轨道上电子数相等;B是短周期中原子半径最大的元素;C元素3p能级半充满;E是所在周期电负性最大的元素;F是第四周期未成对电子最多的元素。
试回答下列有关的问题:
(1)写出F元素的电子排布式:________________。
(2)已知A元素的一种氢化物分子中含四个原子,则在该化合物的分子中A原子的杂化轨道类型为__________。
(3)已知C、E两种元素形成的化合物通常有CE3、CE5两种。这两种化合物中一种为非极性分子,一种为极性分子,属于极性分子的化合物的分子立体构型是________________。
(4)B、C、D、E的第一电离能由大到小的顺序是________(写元素符号)。四种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序是________________(写化学式)。
(5)由B、E两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如下图所示为B、E形成化合物的晶胞结构图以及晶胞的剖面图:

晶胞中距离一个B+最近的B+有________个。若晶体密度为ρ g·cm-3,阿伏加德罗常数的值用NA表示,则E-的离子半径为________cm(用含NA与ρ的式子表达)。
查看答案和解析>>
科目: 来源:2014年高考化学考前题型专练 保温训练(二)(解析版) 题型:填空题
[有机化学基础]塑化剂是工业上被广泛使用的高分子材料助剂,在塑料加工中添加这种物质,可以使其柔韧性增强,容易加工。塑化剂可合法用于工业生产,但禁止作为食品添加剂。截止2011年6月8日,台湾被检测出含塑化剂食品已达961种,据媒体报道,2012年岁末,我国大陆多种著名品牌白酒也陷入了塑化剂风波。
常见塑化剂为邻苯二甲酸酯类物质,某有机物J(C19H20O4)是一种塑料工业中常用的塑化剂,可用下列合成路线合成。
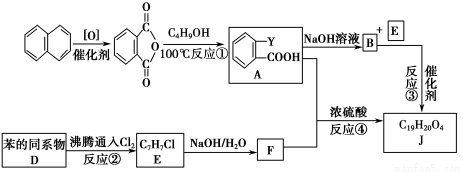
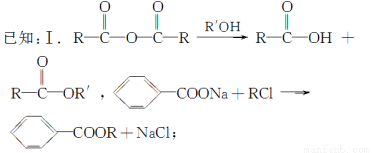
Ⅱ.控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应;
Ⅲ.F与浓溴水混合不产生白色沉淀。
请回答下列问题:
(1)E中官能团的名称为________;F中官能团的电子式为________。
(2)写出A+F→J的化学反应方程式:____________________________
(3)写出下列化学反应类型:
反应①______________________; 反应④__________________。
(4)写出F的属于芳香烃衍生物的同分异构体的结构简式:______________。
(5)C4H9OH的同分异构体中属于醇类的有________种,写出其中具有手性碳的同分异构体的结构简式:____________。
(6)以含碳原子数不同的苯的同系物为原料,可以合成不同种类的塑化剂。教材中苯及其同系物的通式是CnH2n-6(n≥6),某同学根据等差数列公式推导出该系列的通式却是Cn+5H2n+4,老师告诉该同学他推导出的通式也是正确的,但其中n的意义和取值范围与教材中的通式不同,请问:通式Cn+5H2n+4中n的意义是________,其取值范围是________
查看答案和解析>>
科目: 来源:2014年高考化学苏教版一轮复习1-1-1化学实验仪器及操作练习卷(解析版) 题型:选择题
下列有关技术手段或仪器在化学研究中的应用的说法不正确的是 ( )。
A.用电子天平可直接称出某个分子或原子的质量
B.用pH计测定溶液的pH
C.用移液管量取25.00 mL溶液
D.用量热计测定某些化学反应的反应热
查看答案和解析>>
科目: 来源:2014年高考化学苏教版一轮复习1-1-1化学实验仪器及操作练习卷(解析版) 题型:选择题
下列实验中指定使用的仪器必须预先干燥的是 ( )。
①中和热测定实验所用的小烧杯
②中和滴定实验所用的锥形瓶
③配制一定物质的量浓度溶液的实验所用的容量瓶
④喷泉实验用于收集NH3的烧瓶
A.①② B.①④ C.②③ D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com