
科目: 来源:2013-2014学年高考化学二轮复习提分训练 专题14实验化学(选修)练习卷(解析版) 题型:选择题
下列说法不正确的是( )。
A.利用分液漏斗进行分液操作时,先打开分液漏斗旋塞,使下层液体慢慢流出,待下层液体完全流出后,关闭旋塞,上层液体再从上面倒出
B.用玻璃棒蘸取新制氯水,滴在pH 试纸上,然后与比色卡对照,可测定新制氯水的pH
C.在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用、环形玻璃搅拌棒进行搅拌、酸和碱正好反应、取2~3 次的实验平均值,以达到良好的实验效果
D.固体药品取用:块状固体用镊子夹取,粉末状的用药匙或纸槽转移
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮复习提分训练 专题14实验化学(选修)练习卷(解析版) 题型:选择题
下列说法正确的是( )。
A.将3~4个火柴头浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸和NaNO2溶液,若出现白色沉淀,说明含有氯元素
B.在中和热的测定实验中,应先分别测出盐酸和NaOH溶液的温度,再将氢氧化钠溶液迅速倒入盛有盐酸的量热计中,充分反应后再读出并记录反应体系的最高温度
C.在试管中将一定量的浓硝酸,浓硫酸和苯混合,用酒精灯直接加热几分钟,即可制得硝基苯
D.溶质的溶解度越大,溶液的浓度越高,溶剂的蒸发速度越快,溶液的冷却速度越快,析出的晶体就越细小
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮复习提分训练 专题14实验化学(选修)练习卷(解析版) 题型:实验题
偶氮苯是橙红色晶体,溶于乙醇,微溶于水,广泛应用于染料制造和橡胶工业,以硝基苯、镁粉和甲醇为原料制备偶氮苯的实验步骤如下:
步骤1:在反应器中加入一定量的硝基苯、甲醇和一小粒碘,装上冷凝管,加入少量镁粉,立即发生反应。
步骤2:等大部分镁粉反应完全后,再加入镁粉,反应继续进行,等镁粉完全反应后,加热回流30 min。
步骤3:将所得液体趁热倒入冰水中,并不断搅拌,用冰醋酸小心中和至pH为4~5,析出橙红色固体,过滤,用少量冰水洗涤。
步骤4:用95%的乙醇重结晶。
(1)步骤1中反应不需要加热就能剧烈进行,原因是________________。镁粉分两次加入而不是一次性全部加入的原因是___________________ _____________________________________________________。
(2)步骤3中析出固体用冰水洗涤的原因是________________。若要回收甲醇,实验所需的玻璃仪器除冷凝管、酒精灯、牛角管(应接管)和锥形瓶外还应有________________________________________________________________。
(3)取0.1 g偶氮苯,溶于5 mL左右的苯中,将溶液分成两等份,分别装于两个试管中,其中一个试管用黑纸包好放在阴暗处,另一个则放在阳光下照射。用毛细管各取上述两试管中的溶液点在距离滤纸条末端1 cm处,再将滤纸条末端浸入装有1∶3的苯环己烷溶液的容器中,实验操作及现象如下图所示:

①实验中分离物质所采用的方法是________法。
②由实验结果可知:________________;利用该方法可以提纯反式偶氮苯。
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮复习提分训练 专题14实验化学(选修)练习卷(解析版) 题型:实验题
苯甲酸常用于抗真菌及消毒防腐。实验室常用高锰酸钾氧化甲苯制备苯甲酸,其装置如图甲所示(加热、搅拌和仪器固定装置均已略去)。实验过程如下:
①将5.4 mL甲苯、100 mL水、几粒沸石加入250 mL三颈烧瓶中;
②装上冷凝管,加热至沸后分批加入16 g高锰酸钾,回流反应4 h;
③将反应混合物趁热减压过滤,并用热水洗涤滤渣,将洗涤液并入滤液中;
④滤液加入盐酸酸化后,抽滤(装置如图乙)、洗涤、干燥得苯甲酸粗产品。
在苯甲酸制备过程中发生反应:
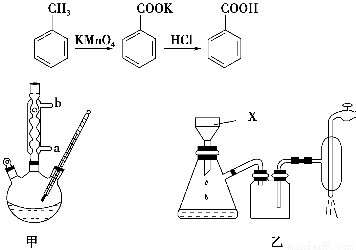
(1)图甲冷凝管中冷水应从________(填“a”或“b”)管进入,图乙中仪器X的名称为________。
(2)实验中分批加入KMnO4的原因是_________________________。
(3)判断甲苯被氧化完全的实验现象是___________________________。
(4)抽滤操作与普通过滤相比,除了得到沉淀较干燥外,还有一个优点是__________________________________________________________。
(5)第一次过滤时,若溶液呈红色,可加入下列试剂处理________(填字母)。
A.H2O B.CCl4
C.NaHSO3 D.HNO3
(6)苯甲酸在不同温度下溶解度见下表:
T/℃ | 4 | 18 | 75 |
溶解度/g | 0.18 | 0.27 | 2.20 |
洗涤苯甲酸晶体时应用________洗涤。
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮复习提分训练 专题14实验化学(选修)练习卷(解析版) 题型:实验题
邻叔丁基对苯二酚(TBHQ)是一种新颖的食品抗氧剂,其制备原理如下:


实验过程中的主要步骤如下:
步骤1:向三颈烧瓶中加入5.5 g对苯二酚,5.0 mL浓磷酸及20 mL二甲苯(装置如图所示),启动搅拌器。

步骤2:缓缓加热到100~110 ℃,慢慢滴加7.5 mL叔丁醇和5 mL二甲苯组成的溶液,30~60 min内滴完。
步骤3:升温到135~140 ℃,恒温回流2.5 h。
步骤4:将反应液冷却到120 ℃,直到反应完成。
步骤5:将反应液倒入烧杯,并用热水洗涤三颈烧瓶,洗液并入烧杯中。
步骤6:冷却结晶,抽滤,回收滤液中的二甲苯和磷酸。
步骤7:用干甲苯重结晶、脱色、冷水洗涤、干燥。
(1)磷酸在实验中的作用是________。
(2)本实验中二甲苯的作用是_________________________________ __________________________________________________。
(3)步骤4中反应完成的标志是_________________________。
(4)步骤7脱色时,可用的脱色剂是________。
(5)对合成得到的产品表征,还需要的主要现代分析仪器是__________________________。
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮复习提分训练 专题2化学常用计量练习卷(解析版) 题型:选择题
下列说法中正确的是( )
A.2 mol CH4 的质量和O2的摩尔质量都是32 g
B.1 mol任何气体中都含有相同的原子数
C.0.5 mol NaCl约含有6.02×1023个离子
D.1 mol·L-1 KCl溶液中含有溶质1 mol
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮复习提分训练 专题2化学常用计量练习卷(解析版) 题型:选择题
下列说法正确的是( )。
A.分子数不同的CO与N2的体积一定不等
B.体积相同的CO与N2的质量一定相等
C.质量相同、密度不同的CO与N2所含的原子数目一定相等
D.质量不同、密度相同的CO与N2所含分子数可能相同
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮复习提分训练 专题2化学常用计量练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是( )。
A.某温度下,1 L pH=8的纯水中含OH-为10-8NA
B.14 g分子通式为CnH2n的链烃中含有的C=C键数目为NA
C.标准状况下,22.4 L Cl2与足量Fe反应,转移的电子数为3NA
D.常温下,1 L 0.1 mol·L-1 CH3COONa溶液中含有的Na+和CH3COO-总数为0.2NA
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮复习提分训练 专题2化学常用计量练习卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值,下列叙述正确的是( )。
A.10 g氖气中所含的原子数为NA
B.9 g重水含有的电子数为5 NA
C.标准状况下,将22.4 L氯化氢气体溶于足量水中,溶液中含有的氯化氢分子数为NA
D.常温常压下,22 g CO2中含有NA个C=O键
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮复习提分训练 专题2化学常用计量练习卷(解析版) 题型:选择题
某溶液中大量存在以下浓度的五种离子:0.2 mol·L-1 Cl-、0.4 mol·L-1 SO42-、0.1 mol·L-1 Al3+、0.3 mol·L-1 H+、M,则M及其物质的量浓度可能为( )。
A.Na+ 0.3 mol·L-1 B.Zn2+ 0.2 mol·L-1
C.CO32- 0.2 mol·L-1 D.Ca2+ 0.1 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com