
科目: 来源:山西省模拟题 题型:填空题
 发生如下反应:
发生如下反应: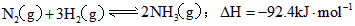 ;
;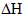 的含义是(填序号):___________。
的含义是(填序号):___________。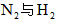 与反应生成
与反应生成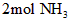 时放出的热量
时放出的热量 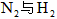 与反应生成
与反应生成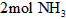 时吸收的热量
时吸收的热量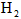 的转化率__________,化学反应速率_____
的转化率__________,化学反应速率_____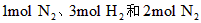 、
、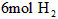 。平衡后,两容器内放出的热量分别记作
。平衡后,两容器内放出的热量分别记作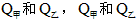 的关系是__________。
的关系是__________。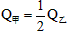 B.
B.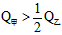 C.
C.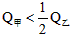 D.无法确定
D.无法确定 查看答案和解析>>
科目: 来源:模拟题 题型:填空题
 2NH3(g);△H=-92.2 kJ/mol。
2NH3(g);△H=-92.2 kJ/mol。
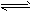 H2(g) +CO(g);△H=+131.3 kJ/mol
H2(g) +CO(g);△H=+131.3 kJ/mol  H2(g)+I2(g)达到平衡后,平衡时I2的浓度c(I2)A____c(I2)B;平衡时HI的分解率
H2(g)+I2(g)达到平衡后,平衡时I2的浓度c(I2)A____c(I2)B;平衡时HI的分解率查看答案和解析>>
科目: 来源:0107 期中题 题型:单选题
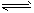 2NH3(g),反应达到平衡后,改变下述条件,NH3气体平衡浓度不改变的是
2NH3(g),反应达到平衡后,改变下述条件,NH3气体平衡浓度不改变的是 查看答案和解析>>
科目: 来源:专项题 题型:填空题
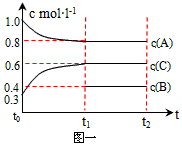
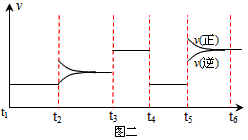
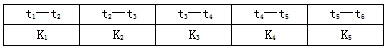
查看答案和解析>>
科目: 来源:0116 期末题 题型:单选题
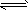 PCl3+Cl2测得压强为P1,此时向反应器中再通入amolPCl5,在温度不变的情况下再度达到平衡,测得压强为P2。则P1和P2的关系是
PCl3+Cl2测得压强为P1,此时向反应器中再通入amolPCl5,在温度不变的情况下再度达到平衡,测得压强为P2。则P1和P2的关系是[ ]
查看答案和解析>>
科目: 来源:浙江省模拟题 题型:填空题
 CO2(g)+H2(g) 将部分CO转换成H2。将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应,得到如下三组数据
CO2(g)+H2(g) 将部分CO转换成H2。将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应,得到如下三组数据
查看答案和解析>>
科目: 来源:吉林省期末题 题型:填空题
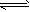 2Z(g) △H<0,在500℃时将2molX和1molY 装入一个体积恒定的10 L密闭容器中,
2Z(g) △H<0,在500℃时将2molX和1molY 装入一个体积恒定的10 L密闭容器中,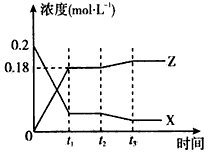
查看答案和解析>>
科目: 来源:专项题 题型:单选题
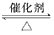 2SO3,平衡时SO3为a mol,在相同温度下分别按下列配比在V L密闭容器中放入起始物质,平衡时有关SO3的物质的量叙述正确的是
2SO3,平衡时SO3为a mol,在相同温度下分别按下列配比在V L密闭容器中放入起始物质,平衡时有关SO3的物质的量叙述正确的是查看答案和解析>>
科目: 来源:专项题 题型:不定项选择题
查看答案和解析>>
科目: 来源:专项题 题型:单选题
 3C(g)+D(g)达平衡时,C的浓度为Wmol/L。若维持容器体积和温度不变,按下列四种配比作为起始物质,达平衡后,C的浓度仍为Wmol/L的是
3C(g)+D(g)达平衡时,C的浓度为Wmol/L。若维持容器体积和温度不变,按下列四种配比作为起始物质,达平衡后,C的浓度仍为Wmol/L的是 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com