
科目: 来源:期末题 题型:填空题
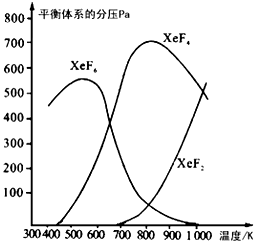
 XeF4(g)+ F2(g),其反应热△H ____(填“>”“=”或“<”)0。理由是______________________。
XeF4(g)+ F2(g),其反应热△H ____(填“>”“=”或“<”)0。理由是______________________。 查看答案和解析>>
科目: 来源:山东省期中题 题型:单选题
 zC(g);平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol/L。下列有关判断正确的是
zC(g);平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol/L。下列有关判断正确的是A.x+y<z
B.平衡向正反应方向移动
C.B的转化率降低
D.C的体积分数增大
查看答案和解析>>
科目: 来源:山东省期中题 题型:单选题
A. ①②③
B. ④⑤
C. ①⑤
D. ⑤
查看答案和解析>>
科目: 来源:山东省期中题 题型:单选题
 2NH3(g);△H<0,下列研究目的和示意图相符的是
2NH3(g);△H<0,下列研究目的和示意图相符的是



查看答案和解析>>
科目: 来源:山东省期中题 题型:单选题
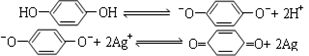 ,能使显影速度明显加快的添加剂是
,能使显影速度明显加快的添加剂是 A.KBr
B.Na2CO3
C.CH3COOH
D.H2O
查看答案和解析>>
科目: 来源:安徽省高考真题 题型:单选题
 2CO2(g)+S(l) △H<0若反应在恒容的密闭容器中进行,下列有关说法正确的是
2CO2(g)+S(l) △H<0若反应在恒容的密闭容器中进行,下列有关说法正确的是 查看答案和解析>>
科目: 来源:江苏高考真题 题型:不定项选择题

查看答案和解析>>
科目: 来源:上海高考真题 题型:填空题
 Si3N4(s)+12HCl(g)+Q(Q>0)
Si3N4(s)+12HCl(g)+Q(Q>0)  ,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比___
,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比___ (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。 查看答案和解析>>
科目: 来源:四川省高考真题 题型:单选题
 2SO3;△H<0。当气体的物质的量减少0.315mol时反应达到平衡,在相同的温度下测得气体压强为反应前的82.5%。下列有关叙述正确的是
2SO3;△H<0。当气体的物质的量减少0.315mol时反应达到平衡,在相同的温度下测得气体压强为反应前的82.5%。下列有关叙述正确的是 查看答案和解析>>
科目: 来源:山西省模拟题 题型:填空题
 CO(g)+H2(g);ΔH=_____________________。(用含ΔH1、ΔH2的代数式表示)
CO(g)+H2(g);ΔH=_____________________。(用含ΔH1、ΔH2的代数式表示) CH3OH(g);ΔH3。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1mol CO和2mol H2的混合气体,控温,进行实验,测得相关数据如下图1和图2。
CH3OH(g);ΔH3。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1mol CO和2mol H2的混合气体,控温,进行实验,测得相关数据如下图1和图2。 

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com