
科目: 来源:专项题 题型:填空题
 CH3OCH3(g)+CO2(g) △H=-246. 4 kJ/mol
CH3OCH3(g)+CO2(g) △H=-246. 4 kJ/mol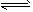 CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:
CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:查看答案和解析>>
科目: 来源:北京期末题 题型:填空题

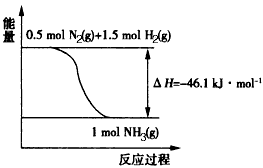
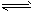 2NH3。
2NH3。查看答案和解析>>
科目: 来源:山东省模拟题 题型:单选题
 2HI(g),在温度T1和T时,产物的量和时间的关系如图所示,根据图象判断正确的是
2HI(g),在温度T1和T时,产物的量和时间的关系如图所示,根据图象判断正确的是 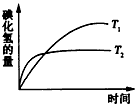
查看答案和解析>>
科目: 来源:山东省模拟题 题型:单选题
 恒容时,若温度适当降低,F的浓度增加。下列说法中正确的是
恒容时,若温度适当降低,F的浓度增加。下列说法中正确的是  A(g)+2B(g)
A(g)+2B(g) 查看答案和解析>>
科目: 来源:河南省模拟题 题型:单选题
查看答案和解析>>
科目: 来源:江西省模拟题 题型:单选题
 I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度与温度T的关系如图所示(曲线上任何一点均表示平衡状态),下列说法正确的是
I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度与温度T的关系如图所示(曲线上任何一点均表示平衡状态),下列说法正确的是
 I3-(aq) △H >0
I3-(aq) △H >0查看答案和解析>>
科目: 来源:0114 模拟题 题型:填空题
 (3+2x)N2+6xH2O
(3+2x)N2+6xH2O 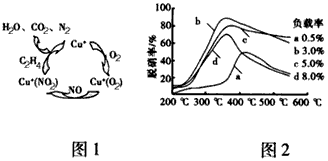
查看答案和解析>>
科目: 来源:0114 模拟题 题型:单选题

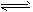 B(g)+2C(g) △H=+100a kJ/mol
B(g)+2C(g) △H=+100a kJ/mol 查看答案和解析>>
科目: 来源:0114 模拟题 题型:填空题
查看答案和解析>>
科目: 来源:浙江省模拟题 题型:单选题
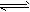 2XY(g) △H<0,达到甲平衡。下面的三个图形表示了在仅改变某一条件后,达到乙平衡的情况,对此过程的分析正确的是
2XY(g) △H<0,达到甲平衡。下面的三个图形表示了在仅改变某一条件后,达到乙平衡的情况,对此过程的分析正确的是 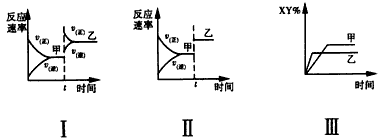
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com