
科目: 来源:肇庆二模 题型:问答题
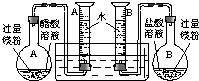
| A烧瓶中 | B烧瓶中 | 20℃、101kPa 50mL量筒内气体读数 |
反应时间 | |
| A瓶 | B瓶 | |||
| 40mL0.1mol/L 醋酸溶液 |
40mL0.1mol/L 盐酸溶液 |
5mL | t(a1)=155s | t(b1)=7s |
| 10mL | t(a2)=310s | t(b2)=16s | ||
| 15mL | t(a3)=465s | t(b3)=30s | ||
| 20mL | t(a4)=565s | t(b4)=64s | ||
| … | … | … | ||
| 44.8mL | t(an)=865s | t(bn)=464s | ||
查看答案和解析>>
科目: 来源:不详 题型:多选题
| A.亚磷酸中磷呈+3价 |
| B.亚磷酸有氧化性和还原性 |
| C.亚磷酸是三元酸 |
| D.亚磷酸只形成两种酸式盐而无正盐 |
查看答案和解析>>
科目: 来源:天津 题型:单选题
| A.CH3 COOH 溶液中离子浓度的关系满足:c(H+)═c(OH-)+c(CH3 COO-) |
| B.0.1 mol?L-1的CH3 COOH 溶液加水稀释,溶液中c(OH-)减小 |
| C.CH3COOH 溶液中加入少量CH3COONa固体,平衡逆向移动 |
| D.常温下,pH=2的CH3COOH 溶液与pH=12的NaOH 溶液等体积混合后,溶液的pH<7 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
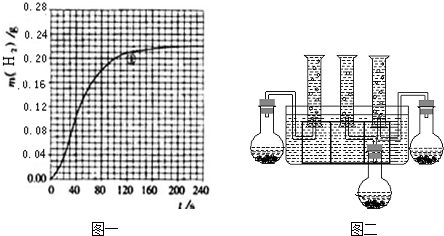
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.(2)(4)(5)(6) | B.(2)(3)(5)(6) | C.(3)(4)(5)(6) | D.全是 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
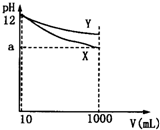
| A.X、Y两种碱的物质的量浓度一定相等 |
| B.若10<a<12,则X、Y都是弱碱 |
| C.完全中和X、Y两溶液时,消耗同浓度盐酸的体积VX>VY |
| D.稀释后,X溶液的碱性比Y溶液的碱性强 |
查看答案和解析>>
科目: 来源:黄浦区二模 题型:多选题
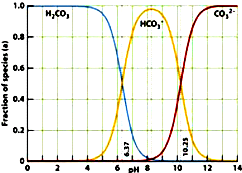
| A.pH=2时,H2CO3、HCO3-、CO32-共存 |
| B.在pH为6.37及10.25时,溶液中c(H2CO3)=c(HCO3-)=c(CO32-) |
| C.人体血液的pH约为7.4,则CO2在血液中多以HCO3-的形式存在 |
| D.若用CO2和NaOH反应制取Na2CO3,溶液的pH必须控制在12以上 |
查看答案和解析>>
科目: 来源:不详 题型:多选题
| A.①中水的电离程度最小,③中水的电离程度最大 |
| B.将②、③混合,若有pH=7,则消耗溶液的体积:②>③ |
| C.将①、④混合,若有c(CH3COO-)>c(H+),则混合液一定呈碱性 |
| D.将四份溶液稀释相同倍数后,溶液的pH:③>④,①>② |
查看答案和解析>>
科目: 来源:朝阳区一模 题型:单选题
| A.分别中和等体积、等pH的盐酸和醋酸,消耗的NaOH物质的量相同 |
| B.常温下,等物质的量浓度的(NH4)2CO3和Na2CO3溶液,前者的c(HCO3-)小 |
| C.NaHCO3溶液中离子浓度有如下关系:c(CO32-)+c(OH-)=c(H+)+c(H2CO3) |
| D.等物质的量浓度、等体积的NaX和弱酸HX溶液混合后,各粒子浓度关系是:c(Na+)>c(HX)>c(X-)>c(OH-)>c(H+) |
查看答案和解析>>
科目: 来源:漳州二模 题型:单选题
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7K2=5.6×10-11 |
| A.等物质的量浓度的各溶液pH关系为:CH3COONa>Na2CO3>NaCN |
| B.a mol/L NaOH溶液与b mol/LHCN溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b |
| C.在冰醋酸中逐滴加水,则溶液的导电性和醋酸的电离程度均先增大后减小 |
| D.NaHCO3和Na2CO3混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com