
科目: 来源:不详 题型:单选题
| A.CO32-+2H2O?H2CO3+2OH- |
| B.Fe3++3H2O?Fe(OH)3↓+3H+ |
| C.CH3COO-+H2O?CH3COOH+OH- |
| D.NH3+H2O?NH3?H2O |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.①② | B.③④ | C.①②④ | D.全部 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.NH4++2H2O?NH3?H2O+H3O+ |
| B.HCO3-+H2O?H3O++CO32- |
| C.HS-+H+═H2S |
| D.Cl2+H2O?H++Cl-+HClO |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.已知常温下0.1 mol?L-1NaCN溶液的pH=12,则已水解的CN-约占总数的10% | ||||
| B.已知25℃时NH4CN溶液显碱性,则25℃时的电离常数K(NH3?H2O)>K(HCN) | ||||
C.NH4ClO4溶液中,c(Cl
| ||||
D.欲使0.1 mol?L-1Na2S溶液中
|
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| 化学式 | 电离常数 |
| HClO | K1=3×10-8 |
| H2CO3 | K2=4.3×10-7 |
| K3=5.6×10-11 |
A.用坩埚灼烧MgCl2?6H2O的反应式 MgCl2?6H2O
| ||||
| B.根据表中提供的数据,等物质的量浓度的NaClO、NaHCO3混合溶液中,有c(HCO3-)>c(ClO-)>c(OH-) | ||||
| C.常温下,将pH=2的稀硫酸稀释10倍,其中各离子的物质的量浓度都变为原来的十分之一 | ||||
D.某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,溶度积常数Ksp=c(Ba2+)?c(SO42-).则加入Na2SO4可使溶液由a点变到b点;通过蒸发可以使溶液由d 点变到c 点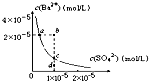 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:济南一模 题型:问答题
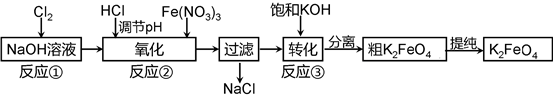
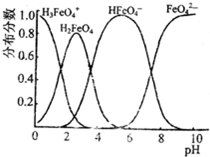
查看答案和解析>>
科目: 来源:同步题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com