
科目: 来源:广东省模拟题 题型:单选题

查看答案和解析>>
科目: 来源:模拟题 题型:单选题
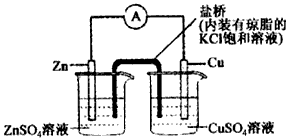
查看答案和解析>>
科目: 来源:天津模拟题 题型:填空题
 CH3OCH3(g)+3H2O(g) △H
CH3OCH3(g)+3H2O(g) △H

查看答案和解析>>
科目: 来源:专项题 题型:单选题

查看答案和解析>>
科目: 来源:专项题 题型:单选题
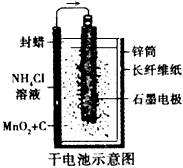
查看答案和解析>>
科目: 来源:北京期末题 题型:单选题
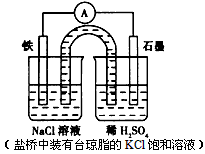
查看答案和解析>>
科目: 来源:河南省模拟题 题型:单选题
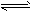 AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2 均为石墨电极),分别进行下述操作:
AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2 均为石墨电极),分别进行下述操作: 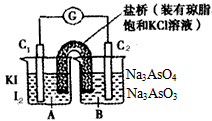
查看答案和解析>>
科目: 来源:河南省模拟题 题型:填空题
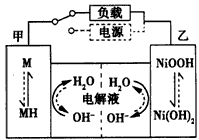
②根据所给信息判断,混合动力车下坡或刹车时,甲电极的电极反应式为_________________;混合动力车上坡或加速时,乙电极的电极反应式为____________________
(3)汽车尾气中的一氧化碳是大气污染物,可通过如下反应降低其浓度:CO(g) +1/2O2(g)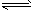 CO2(g)
CO2(g)
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正、逆反应速率关系如下表所 示。请填写表中的空格。
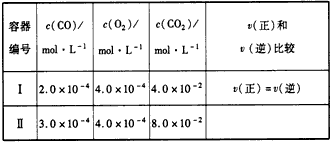
查看答案和解析>>
科目: 来源:模拟题 题型:单选题
 Fe(OH)2+Ni(OH)2,下列有关该电池的说法正确的是
Fe(OH)2+Ni(OH)2,下列有关该电池的说法正确的是 查看答案和解析>>
科目: 来源:模拟题 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com