
科目: 来源:广东省高考真题 题型:单选题
查看答案和解析>>
科目: 来源:浙江省高考真题 题型:单选题
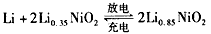
查看答案和解析>>
科目: 来源:福建省高考真题 题型:单选题
 2Fe2+ +I2设计成如下图所示的原电池。下列判断不正确的是
2Fe2+ +I2设计成如下图所示的原电池。下列判断不正确的是 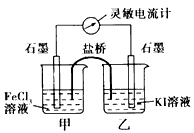
查看答案和解析>>
科目: 来源:四川省高考真题 题型:填空题
新型锂离子电池在新能源的开发中占有重要地位,可用作节能环保电动汽车的动力电池。磷酸亚铁锂(LiFePO4)新型锂离子电池的首选电极材料,它的制备方法如下:
方法一:将碳酸锂、乙酸亚铁[( CH3COO)2Fe]磷酸二氢铵按一定比例混合、充分研磨后,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂,同时生成的乙酸及其他产物均以气体逸出。
方法二:将一定浓度的磷酸二氢铵、氯化锂混合溶液作为电解液,以铁棒为阳极,石墨为阴极,电解析出磷酸亚铁锂沉淀。沉淀经过滤、洗涤、干燥,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂。在锂离子电池中,需要一种有机聚合物作为正负极之间锂离子迁移的介质,该有机聚合物的单体之一(用M表示)的结构简式如下: 
请回答下列问题:
(1)上述两种方法制备磷酸亚铁锂的过程都必须在惰性气体氛围中进行。其原因是________。
(2)在方法一所发生的反应中,除生成磷酸亚铁锂、乙酸外,还有 ___ 、____、____ (填化学式)生成。
(3)在方法二中,阳极生成磷酸亚铁锂的电极反应式为____。
(4)写出M与足量氢氧化钠溶液反应的化学方程式:___。
(5)已知该锂离子电池在充电过程中,阳极的磷酸亚铁锂生成磷酸铁,则该电池放电时正极的电极反应式为_______________________。
查看答案和解析>>
科目: 来源:0112 期中题 题型:填空题

查看答案和解析>>
科目: 来源:浙江省期末题 题型:单选题

查看答案和解析>>
科目: 来源:0104 期中题 题型:单选题
查看答案和解析>>
科目: 来源:0104 期中题 题型:单选题
查看答案和解析>>
科目: 来源:0104 期中题 题型:填空题
查看答案和解析>>
科目: 来源:0113 期末题 题型:填空题
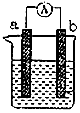
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com