
科目: 来源:0110 模拟题 题型:填空题
 CO(g)+2H2(g);△H= -36kJ/mol ①
CO(g)+2H2(g);△H= -36kJ/mol ①  CO(g)+3H2(g);△H= +216kJ/mol ②
CO(g)+3H2(g);△H= +216kJ/mol ②  CO(g)+3H2(g)。当甲烷的转化率为0.5时,此时平衡常数为__________。
CO(g)+3H2(g)。当甲烷的转化率为0.5时,此时平衡常数为__________。 Na2FeO2+H2O+NH3↑ ①;
Na2FeO2+H2O+NH3↑ ①; 4Na2Fe2O4+3NH3↑ ②;
4Na2Fe2O4+3NH3↑ ②;
查看答案和解析>>
科目: 来源:重庆市高考真题 题型:填空题
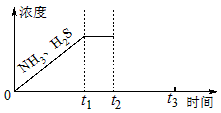
查看答案和解析>>
科目: 来源:专项题 题型:单选题

查看答案和解析>>
科目: 来源:模拟题 题型:填空题
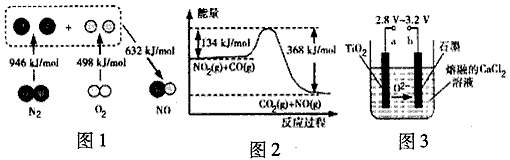
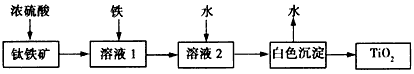
①溶液2加水稀释,可使TiO2+水解生成白色沉淀TiO(OH)2,原因是_______________。
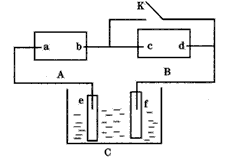
②工业上在800℃~1 000℃下,电解TiO2可制得海绵钛,其装置示意图如上图3。写出其阴极的电极反应式:_____________________。
查看答案和解析>>
科目: 来源:模拟题 题型:填空题
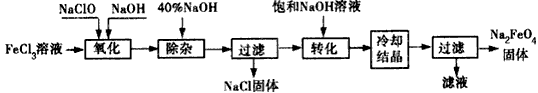
查看答案和解析>>
科目: 来源:北京高考真题 题型:填空题
查看答案和解析>>
科目: 来源:同步题 题型:填空题
查看答案和解析>>
科目: 来源:同步题 题型:计算题
查看答案和解析>>
科目: 来源:同步题 题型:填空题

查看答案和解析>>
科目: 来源:模拟题 题型:填空题

 TiCl4(l)+O2(g) △H=+151 kJ.mol-1难于发生,所以工业上不能直接由TiO2和
TiCl4(l)+O2(g) △H=+151 kJ.mol-1难于发生,所以工业上不能直接由TiO2和 TiCl4 (l) +2CO( g) △H2 则△H2=____。
TiCl4 (l) +2CO( g) △H2 则△H2=____。 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com