
科目: 来源:2015届湖北省孝感市七校联考高二下学期期中考试化学试卷(解析版) 题型:选择题
对充有氖气的霓虹灯管通电,灯管发出红色光。产生这一现象的主要原因( )
A.在电流的作用下,氖原子与构成灯管的物质发生反应
B.电子由基态向激发态跃迁时吸收除红光以外的光线
C.氖原子获得电子后转变成发出红光的物质
D.电子由激发态向基态跃迁时以光的形式释放能量
查看答案和解析>>
科目: 来源:2015届湖北省孝感市七校联考高二下学期期中考试化学试卷(解析版) 题型:选择题
某元素的原子最外电子层排布是5s25p1,该元素或其化合物不可能具有的性质是 ( )
A.该元素单质是导体
B.该元素单质在一定条件下能与盐酸反应
C.该元素的最高化合价呈+5价
D.该元素的氧化物的水合物显碱性
查看答案和解析>>
科目: 来源:2015届湖北省孝感市七校联考高二下学期期中考试化学试卷(解析版) 题型:选择题
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为 ( )
A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。
B.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。
C.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。
D.氨气分子是极性分子而甲烷是非极性分子。
查看答案和解析>>
科目: 来源:2015届湖北省孝感市七校联考高二下学期期中考试化学试卷(解析版) 题型:填空题
M原子在第二能层上只有一个空轨道,则M是 ;其电子排布式为 ;R原子的3p轨道上只有一个未成对电子,则R原子可能是 、 ;Y原子的核电荷数为33,其外围电子排布是 ,其在元素周期表中的位置是 ,是属于 区的元素。
查看答案和解析>>
科目: 来源:2015届湖北省孝感市七校联考高二下学期期中考试化学试卷(解析版) 题型:填空题
运送“神舟五号”飞船的火箭燃料除液态双氧水外,还有另一种液态氮氢化合物。已知该化合物中氢元素的质量分数为12. 5%,相对分子质量为32,结构分析发现该分子结构中只有单键。
(1)该氮氢化合物的电子为 。
(2)若该物质与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,写出该反应的化学方程式 。
(3)NH3分子中的N原子有一对孤对电子,能发生反应:NH3+HCl=NH4Cl。试写出上述氮氢化合物通入足量盐酸时,发生反应的化学方程式
查看答案和解析>>
科目: 来源:2015届湖北省孝感市七校联考高二下学期期中考试化学试卷(解析版) 题型:填空题
氮可以形成多种离子,如N3-,NH2-,N3-,NH4+,N2H5+,N2H62+等,已知N2H5+
与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于 NH4+的性质。
⑴写出N2H62+在碱性溶液中反应的离子方程式 。
⑵NH2-的电子式为 。
⑶N3-有 个电子。
⑷写出二种由多个原子组成的含有与N3-电子数相同的物质的化学式 、 。
⑸等电子数的微粒往往具有相似的结构,试预测N3—的构型 。
⑹据报道,美国科学家卡尔·克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。则“N5”分子碎片所带电荷是 。
查看答案和解析>>
科目: 来源:2015届湖北省孝感市七校联考高二下学期期中考试化学试卷(解析版) 题型:填空题
下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
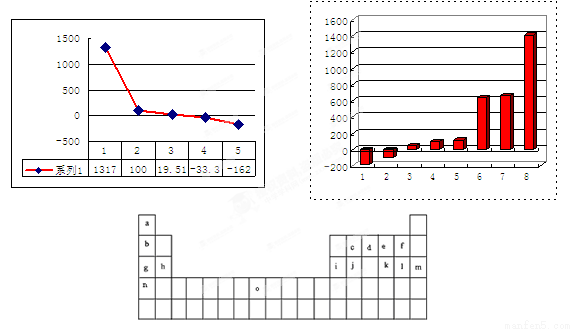
试回答下列问题
(1)元素“O”在周期表中的位置是 。
(2)画出“c”的简化电子排布式 。
(3)第三周期8种元素按单质熔点大小顺序的柱形图如上,其中序列“1”代表 (填字母)。
(4)b、c、d、e、f的氢化物的沸点(℃)直角坐标图如右,序列“5”氢化物的化学式为: ;序列“1”氢化物的电子式为: 。
查看答案和解析>>
科目: 来源:2015届湖北省孝感市七校联考高二下学期期中考试化学试卷(解析版) 题型:填空题
X、Y、W、M、N五种元素分别位于周期表中三个紧邻的周期,且原子序数逐渐增大,X和Y的氢化物都比同族元素氢化物的沸点高,但在同周期中却不是最高的。W是同周期元素中离子半径最小的元素。M原子的最外能层上有两个运动状态不同的电子。N是一种“明星金属”,广泛应用于航天、军事等工业领域。请回答下列问题:
⑴X、Y两种元素的元素符号是: 、 。X、Y可以形成一种共价化合物,其中两种元素最外层电子数都达到8,则其分子的空间构型是: ;中心原子的杂化方式是: 。
⑵X的氢化物易溶于水的其原因是: 。
⑶N的电子排布式是: 。
⑷X和Y两元素的第一电离能大小关系: 小于 (填元素符号)。
查看答案和解析>>
科目: 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
化学与生活、社会密切相关。下列说法不正确的是( )
A.光导纤维导电能力很强,是一种很好的通讯材料
B.纯碱不仅有较强的去油污能力,还可以用于中和发酵面团中的酸性物质
C.煤的气化和液化都属于化学变化
D.钛被誉为“太空金属”,室温下不与水、稀硫酸、稀硝酸反应,却溶于氢氟酸,可能是因为氟离子易与钛离子形成可溶性难电离物质
查看答案和解析>>
科目: 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是( )
A.过氧化钠的电子式: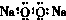
B.质子数为35、中子数为45的溴原子: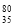 Br
Br
C.硫离子的结构示意图:
D.间二甲苯的结构简式: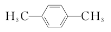
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com