
科目: 来源:2014高考名师推荐化学微粒的组成、结构及性质(解析版) 题型:选择题
A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质。已知:甲+乙=丁+辛,甲+丙=戊+辛;常温下0.1 mol·L-1丁溶液的pH=13。下列说法中正确的是
A.元素B在周期表中的位置为第二周期第ⅥA族
B.元素B、C、D的原子半径由大到小的顺序为r(D)>r(C)>r(B)
C.1.0 L 0.1 mol·L-1戊溶液中阴离子总的物质的量小于0.1 mol
D.1 mol甲与足量的乙完全反应共转移了约6.02×1023个电子
查看答案和解析>>
科目: 来源:2014高考名师推荐化学微粒的组成、结构及性质(解析版) 题型:选择题
两种元素原子的核外电子层数之比与最外层电子数之比相等,则在周期表的前10号元素中,满足上述关系的元素共有
A.1对 B.2对 C.3对 D.4对
查看答案和解析>>
科目: 来源:2014高考名师推荐化学微粒的组成、结构及性质(解析版) 题型:选择题
元素A的阳离子aAm+与元素B的阴离子bBn-具有相同的电子层结构。以下关于A、B元素性质的比较中,正确的是
①原子序数:A>B
②离子半径:aAm+<bBn-
③原子半径:A<B
④元素所在的周期数:A>B
⑤A的最高正价与B的最低负价的绝对值相等
⑥b=a+m-n
A.②③④ B.①②④ C.④⑤⑥ D.②⑤⑥
查看答案和解析>>
科目: 来源:2014高考名师推荐化学微粒的组成、结构及性质(解析版) 题型:选择题
元素的原子结构决定其性质和在周期表中的位置,下列说法中正确的是
A.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
B.某微粒的结构示意简图为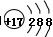 ,则该元素在周期表中位于第三周期、ⅥA族
,则该元素在周期表中位于第三周期、ⅥA族
C.过氧化氢电子式: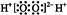
D.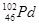 和
和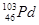 互为同位素
互为同位素
查看答案和解析>>
科目: 来源:2014高考名师推荐化学微粒的组成、结构及性质(解析版) 题型:选择题
下列关于指定粒子构成的叙述中,不正确的是
A.37Cl与39K具有相同的中子数
B.第114号元素的一种核素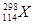 与
与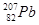 具有相同的最外层电子数
具有相同的最外层电子数
C.H3O+与OH-具有相同的质子数和电子数
D.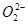 与S2-具有相同的质子数和电子数
与S2-具有相同的质子数和电子数
查看答案和解析>>
科目: 来源:2014高考名师推荐化学微粒的组成、结构及性质(解析版) 题型:填空题
下表为部分短周期元素化合价及相应原子半径的数据:
元素性质 | 元素编号 | |||||||
A | B | C | D | E | F | G | H | |
原子半径(nm) | 0.102 | 0.110 | 0.117 | 0.074 | 0.075 | 0.071 | 0.099 | 0.077 |
最高化合价 | +6 | +5 | +4 |
| +5 |
| +7 | +4 |
最低化合价 | -2 | -3 | -4 | -2 | -3 | -1 | -1 | -4 |
已知:
①A与D可形成化合物AD2、AD3;
②E与D可形成多种化合物,其中ED、ED2 是常见的化合物,C可用于制光电池。
(1)E在周期表中位置是 ;
(2)C和H的气态氢化物的稳定性强弱关系为 (用分子式表示);
(3)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸。该反应的化学方程式是 。
(4)工业上可用纯碱溶液处理ED和ED2,该反应如下:
ED+ED2+Na2CO3=2 +CO2
横线上某盐的化学式应为 。
(5)在一密闭容器中发生反应2AD2+D2 2AD3 ΔH=-47 kJ/mol,在上述平衡体系中加入18D2,当平衡发生移动后,AD2中18D的百分含量 (填“增加”“减少”或“不变”)其原因为 。
2AD3 ΔH=-47 kJ/mol,在上述平衡体系中加入18D2,当平衡发生移动后,AD2中18D的百分含量 (填“增加”“减少”或“不变”)其原因为 。
(6)请设计一个实验方案,使铜和稀的H2AD4溶液反应,得到蓝色溶液和氢气。绘出该实验方案装置图。
查看答案和解析>>
科目: 来源:2014高考名师推荐化学微粒的组成、结构及性质(解析版) 题型:填空题
A、B、C、D、E、F均为短周期主族元素,且原子序数依次增大。短周期元素中C的原子半径最大,B、E同族,E的最外层电子数是电子层数的2倍,A的最高价氧化物水化物为H2AO3,D是地壳中含量最高的金属元素。
(1)A的元素符号是 ,C2B2的电子式为 。
(2)B、C、D、F的离子半径由大到小的顺序是 (用离子符号表示)。
(3)E和F相比,非金属性强的是 (用元素符号表示),下列事实能证明这一结论的是 (用符号填空)。
①常温下E的单质呈固态,F的单质呈气态 ②气态氢化物的稳定性:F>E ③E和F形成的化合物中,E显正价 ④F单质能与E的氢化物发生置换反应 ⑤E和F的氧化物的水化物的酸性强弱 ⑥气态氢化物的还原性:E>F
(4)把CDB2溶液蒸干所得的固体物质为 (填化学式)。
(5)C和F可组成化合物甲,用惰性电极电解甲的水溶液,电解的化学方程式为 。
(6)A、B、C三种元素组成的常见化合物乙的溶液中,离子浓度由大到小的顺序为 ,pH=10的乙溶液中由水电离产生的c(OH-)= mol·L-1。
查看答案和解析>>
科目: 来源:2014高考名师推荐化学探究组成、性质的实验方案的设计与评价(解析版) 题型:选择题
某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
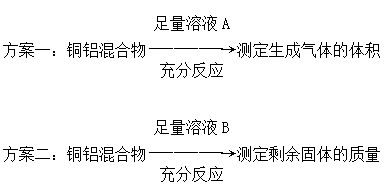
下列有关判断中不正确的是
A.溶液A和溶液B均可以是盐酸或NaOH溶液
B.若溶液B选用浓硝酸,测得铜的质量分数偏大
C.方案一可能产生氢气,方案二可能剩余铜
D.实验室中方案Ⅱ更便于实施
查看答案和解析>>
科目: 来源:2014高考名师推荐化学探究组成、性质的实验方案的设计与评价(解析版) 题型:选择题
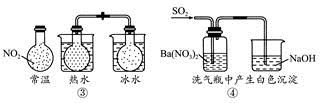
下列实验对应的结论不正确的是
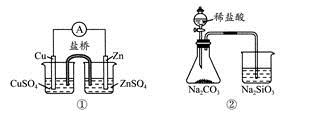
A.①能组成Zn-Cu原电池
B.②能证明非金属性Cl>C>Si
C.③说明反应2NO2(g)  N2O4(g),ΔH<0
N2O4(g),ΔH<0
D.④白色沉淀为BaSO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com